Download Soal dan Pembahasan OSP Kimia 2018 PDF DOC – Pembahasan Soal dan Kunci Jawaban Olimpiade Sains Nasional Tingkat Provinsi 2018 untuk Persiapan OSP 2019 | Postingan ini dirilis di awal bulan Februari 2019. Artinya kurang dari sebulan lagi, penyelenggaraan seleksi OSN Tingkat Kabupaten / Kota atau OSK tahun 2019 dimulai. Untuk Pembahasan Soal OSK 2018 dan 2017 sanggup dilihat di sajian OSK atau linknya saya taruh di bawah ini. Selain mempelajari soal tingkat Kabupaten / Kota, tidak ada salahnya bila mencar ilmu pula soal OSN Tingkat Provinsi atau OSP. Berikut ini Pembahasan Soal dan kunci tanggapan OSP Kimia 2018 khusus pilihan ganda untuk persiapan OSP Kimia 2019. Fisika Biologi Matematika Astronomi Kebumian Geografi Ekonomi Komputer menyusul.
Download Soal dan Pembahasan OSP Kimia 2018 PDF DOC
SOAL DAN PEMBAHASAN OSP KIMIA 2019 klik disini
Baca juga soal dan kunci tanggapan OSK 2017 dan 2018
Download Soal dan Kunci Jawaban OSN 2017 PDF Semua Bidang | Seleksi Tingkat Kabupaten OSK
Download Soal dan Kunci Jawaban OSK 2018 | Semua Bidang Lomba
Baca juga Pembahasan Soal OSK 2018 PDF DOC
Pembahasan Soal OSN Kimia 2018 Tingkat Kabupaten (OSK) PDF
Soal OSP Kimia 2018 Nomer 1 PDF DOC rukim.id
Brom (Br2) diekstrak dari Laut Mati (Dead Sea), ditransportasikan sebagai larutan 52% massa kalsium bromida. Massa brom (dalam ton) yang terkandung dalam 100 ton larutan ini ialah …
A. 15,6 ton
B. 20,8 ton
C. 29,4 ton
D. 41,6 ton
E. 52,0 ton
Pembahasan Soal OSP Kimia 2018 Nomer 1 PDF DOC
Massa molar CaBr2 = (40,08 + 79,90×2) g/mol
Massa molar CaBr2 = 199,88 g/mol
Massa molar Br2 = (79,90×2) g/mol
Massa molar Br2 = 159,80 g/mol
Dengan kadar 52% CaBr2 sebanyak 100 ton larutan terdapat 52 ton CaBr2.
52 ton = 52 × 106 gram
Br2 diekstrak berdasar reaksi:
CaBr2 → Ca2+ + Br2
Dari persamaan reaksi diketahui bahwa setiap jumlah (mol) CaBr2 setara dengan jumlah (mol) Br2
52 ton CaBr2 = 52×106 g / 199,88 g/mol
52 ton CaBr2 = 260.156,09 mol
Jumlah Br2 = jumlah CaBr2
Jumlah Br2 = 260.156,09 mol
Jumlah Br2 = 260.156,09 mol×159,80 g/mol
Jumlah Br2 = 41.572.943,18 g
Jumlah Br2 = 41.572.943,18 g106 g/ton
Jumlah Br2 = 41,572943 ton=41,60 ton
Kunci Jawaban Soal OSP Kimia 2018 Nomer 1 yang sempurna D.
Soal OSP Kimia 2018 Nomer 2 PDF DOC rukim.id
Magnesium sebanyak 2,4 g dimasukkan ke dalam 350 ml larutan HCI 1,0 M. Setelah reaksi selesai, MgCl2 yang terbentuk sebanyak 4,75 gram. Persen hasil MgCI2 adalah:
A. 25
B. 50
C. 75
D. 90
E. 100
Pembahasan Soal OSP Kimia 2018 Nomer 2 PDF DOC
Massa molar Mg = 24,31 g/mol
Massa molar MgCl2 = (24,31 + 35,45×2) g/mol
Massa molar MgCl2 = 95,21 g/mol
Reaksi yang terjadi:
Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
Hitungan stoikiometris:
2,4 g Mg = 2,4 g ÷ 24,31 g/mol
2,4 g Mg = 0,10 mol
350 mL HCl 1 M = 0,35 l × 1 M
350 mL HCl 1 M = 0,35 mol
Secara teori massa MgCl2 seharusnya adalah
0,1 mol × 95,21 g/mol = 9,521 g
Kadar MgCl2 = (massa kasatmata ÷ massa teori) × 100%
Kadar MgCl2 = (4,75 ÷ 9,521) × 100%
Kadar MgCl2 = 49,89% ≈ 50%
Kunci Jawaban Soal OSP Kimia 2018 Nomer 2 yang sempurna B
Lanjut ke halaman 2
Soal OSP Kimia 2018 Nomer 3 PDF DOC rukim.id
Nitrogliserin, suatu materi peledak, terurai sesuai persamaan berikut:
4C3H5(NO3)3(s) → 12CO2(g) + 10H2O(g) + 6N2(g) + O2(g)
Jika 260 g nitrogliserin terurai, maka volume gas yang dihasilkan pada tekanan 1,2 atm dan 270C adalah:
A. 41 L
B. 105 L
C. 130 L
D. 170 L
E. 235 L
Pembahasan Soal OSP Kimia 2018 Nomer 3 PDF DOC
Massa molar C3H5(NO3)3 = 227,09 g/mol
260 g C3H5(NO3)3 = 260 g ÷ 227,09 g/mol
260 g C3H5(NO3)3 = 1,145 mol
Semua hasil reaksi berupa gas dengan total koefisien gas = 12+10+6+1=29
Berdasarkan perbandingan koefisien zat pada persamaan reaksi setara maka
jumlah gas hasil (mol) = 29 × (jumlah C3H5(NO3)3 ÷ 4)
jumlah gas hasil (mol) = 29 × (1,145 mol ÷ 4)
jumlah gas hasil (mol) = 8,30125 mol
Volume gas pada tekanan 1,2 atm dan temperatur 27 oC (= 300 K) sanggup dihitung dengan rumus:
V = (n.R.T) ÷ P
V = (8,30125 mol × 0,08205 L.atm/K.mol × 300 K) ÷ 1,2 atm
V = 170,279390625 L ≈ 170 L
Kunci Jawaban Soal OSP Kimia 2018 Nomer 3 yang sempurna D
Soal OSP Kimia 2018 Nomer 4 PDF DOC
Tekanan osmosis sanggup dipakai untuk memilih berat molekul suatu senyawa dan umumnya dipakai untuk menghitung massa molekul protein. Jika 1,00 g protein dilarutkan dalam 100 ml air, tekanan osmosisnya menjadi 92,90 mm Hg. Massa molekul protein tersebut ialah (asumsi: i = 1 dan suhu 250C):
A. 100
B. 400
C. 1000
D. 2000
E. 4000
Pembahasan Soal OSP Kimia 2018 Nomer 4 PDF DOC
Tekanan osmosis (p)
p = (n/V) × R × T × i
p × V = n × R × T × 1
p × V = massa protein/massa molar protein × R × T
p × V × massa molar protein = massa protein × R × T
massa molar protein = massa protein×R×T / π×V
massa molar protein = 1 g x 0,08205 × 298 / 92,90/760 atm × 100/1000 L
massa molar protein = 24,45090 / 0,0122237 g/mol
massa molar protein = 2000 g/mol
Jadi massa molekul relatif protein tersebut ialah 2000
Kunci Jawaban Soal OSP Kimia 2018 Nomer 4 yang sempurna D
Lanjut ke halaman 3
Soal OSP Kimia 2018 Nomer 5 PDF DOC
Gallium mempunyai konfigurasi elektron [Ar] 3d10 4s24 p1, dengan [Ar] mewakili konfigurasi elektron argon. Urutan pelepasan elektron yang sempurna untuk membentuk ion G4+ adalah:

Pembahasan Soal OSP Kimia 2018 Nomer 5 PDF DOC
Konfigurasi elektron Ga = [Ar] 3d104s24p1
Elektron yang akan terionkan lebih dahulu ialah elektron pada kulit terluar, dalam hal ini ialah kulit ke-4, kemudian gres kulit ke-3. 4p ialah mempunyai energi relatif lebih tinggi dibanding 4s.
Oleh alasannya ialah itu urutan pelepasan elektronnya di mulai dari 4p, 4s, 4s, 3d
Kunci Jawaban Soal OSP Kimia 2018 Nomer 5 yang sempurna E
Download Soal dan Pembahasan OSP Kimia 2018 PDF DOC
Baca juga soal dan kunci tanggapan OSK 2017 dan 2018
Download Soal dan Kunci Jawaban OSN 2017 PDF Semua Bidang | Seleksi Tingkat Kabupaten OSK
Download Soal dan Kunci Jawaban OSK 2018 | Semua Bidang Lomba
Baca juga pembahasan soal OSK 2018 PDF DOC
Pembahasan Soal OSN Kimia 2018 Tingkat Kabupaten (OSK) PDF
Soal OSP Kimia 2018 Nomer 6 PDF DOC
Di antara pasangan molekul berikut ini, yang mengatakan bahwa dipol permanen dalam molekul I lebih besar dibandingkan dalam molekul II adalah:
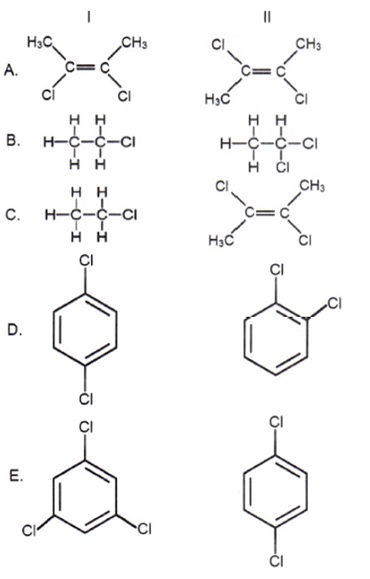
Pembahasan Soal OSP Kimia 2018 Nomer 6 PDF DOC
Dipol permanen terjadi alasannya ialah adanya ikatan atau gaya tarik antara 2 atom yang mempunyai perbedaan keelektronegatifan yang signifikan, dipol permanen terjadi pada molekul yang bersifat polar.
Selain itu geometri molekul (posisi atom-atom dalam molekul) juga memilih kepolaran secara keseluruhan.
Bila resultan gaya tarik dalam molekul saling meniadakan (simetris) maka menghasilkan molekul yang nonpolar atau kurang polar, sedangkan bentuk molekul yang asimetris relatif lebih polar.
Berikut ini kesimpulan wacana dipol permanen yang dibandingkan:
- I > II
- I < II
- I > II
- I < II
- Gugus Cl pada kedua molekul menghasilkan resultan nol
Kunci Jawaban Soal OSP Kimia 2018 Nomer 6 yang sempurna A dan C
Lanjut ke halaman 4
Soal OSP Kimia 2018 Nomer 7 PDF DOC
Berdasarkan struktur senyawa berikut ini:
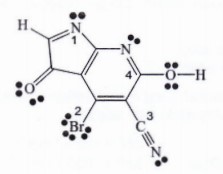
Jumlah ikatan sigma (σ) dan pi (π) dalam struktur senyawa tersebut masing masing adalah:
A. 10 ikatan σ dan 13 ikatan π
B. 13 ikatan σ dan 13 ikatan π
C. 15 ikatan σ dan 6 ikatan π
D. 16 ikatan σ dan 6 ikatan π
E. 17 ikatan σ dan 7 ikatan π
Pembahasan Soal OSP Kimia 2018 Nomer 7 PDF DOC
Setiap ikatan tunggal merupakan ikatan
Setiap ikatan rangkap dua, terdiri dari 1 ikatan dan 1 ikatan
Setiap ikatan rangkap tiga, terdiri dari 1 ikatan dan 2 ikatan
Dalam struktur molekul dalam soal terdiri:
11 ikatan tunggal = 11 ikatan
5 ikatan rangkap dua = 5 ikatan dan 5 ikatan
1 ikatan rangkap tiga = 1 ikatan dan 2 ikatan
Jadi secara keseluruhan dalam molekul terdapat 17 ikatan dan 7 ikatan
Kunci Jawaban Soal OSP Kimia 2018 Nomer 7 yang sempurna E
Soal OSP Kimia 2018 Nomer 8 PDF DOC
Sejak tahun 1850, sebagian besar buku dicetak pada kertas asam yang menyebabkan buku menjadi ringkih dan cepat rusak alasannya ialah mengandung residu asam dan sedikit air yang tertahan di kertas tersebut. Untuk mencegahnya, buku diawetkan dengan mereaksikan kertas dan uap dietilzink, Zn(C2H5)2. Reaksi dietilzink dengan suatu asam HX menghasilkan etana:
Zn(C2H5)2 + 2HX → ZnX2 + 2C2H6.
Produk yang dihasilkan dari reaksi antara dietilzink dengan air adalah:
A. ZnH2 dan C2H6
B. ZnH2 dan C2H5OH
C. Zn(OH)2 dan C2H6
D. Zn(OH)2 dan C2H5OH
E. Zn dan C2H6
Pembahasan Soal OSP Kimia 2018 Nomer 8 PDF DOC
Reaksi antara dietilzink dengan air ini ibarat dengan reaksi yang diberikan pada soal. H–X tipenya ibarat H–OH. Pada HX, X– yang berikatan dengan Zn2+, bila dengan air maka Zn2+ yang berikatan ialah OH–. Sementara itu etil akan berikatan dengan H membentuk etana (C2H6)
Reaksi yang terjadi:
Zn(C2H5)2 + H2O → Zn(OH)2 + 2C2H6
Kunci Jawaban Soal OSP Kimia 2018 Nomer 8 yang sempurna C
Lanjut ke halaman 5
Soal OSP Kimia 2018 Nomer 9 PDF DOC
Reaksi 3O2 → 2O3 berlangsung dengan laju hilangnya O2 setara dengan 0,60 mol/L.det. Besar laju terbentuknya O3 (dalam mol/L.det) adalah:
A. 1,20
B. 0,90
C. 0,60
D. 0,40
E. 0,10
Pembahasan Soal OSP Kimia 2018 Nomer 9 PDF DOC
Reaksi yang terjadi:
3O2 → 2O3
−rO2 = 0,6mol/L
Tanda + dan – hanya dipakai untuk menandai bahwa zat bertambah atau berkurang saja.
Pernyataan laju reaksi di atas sanggup ditulis:
Kunci Jawaban Soal OSP Kimia 2018 Nomer 9 yang sempurna D
Soal OSP Kimia 2018 Nomer 10 PDF DOC
Reaksi 2C4H6 → C8H12, aturan lajunya ialah r = k[C4H6]2. Jika [C4H6] = 2,0 M, laju reaksinya ialah 0,106 M/det. Jika [C4H6] = 4,0 M, maka laju reaksinya adalah:
A. 0,022M/det
B. 0,053 M/det
C. 0, 106 M/det
0. 0,212 M/det
E. 0,424 M/det.
Pembahasan Soal OSP Kimia 2018 Nomer 10 PDF DOC
2C4H6 → C8H12
r = k [C4H6]2
Jika [C4H6] = 2 M → r = 0,106 M/det
k = r ÷ [C4H6]2
k = 0,106 M/det ÷ (2 M)2
k = 0,106 M/det ÷ 4 M2
Jika [C4H6] = 4 M
r = k [C4H6]2
r = (0,106 M/det ÷ 4 M2) × (4 M)2
r = (0,106 M/det ÷ 4 M2) × 16 M2
r = 0,106 M/det × 4 M2
r = 0,424 M/det
Kunci Jawaban Soal OSP Kimia 2018 Nomer 10 yang sempurna E
Lanjut ke halaman 6
Soal OSP Kimia 2018 Nomer 11
Pada masing-masing reaksi kesetimbangan dalam pilihan tanggapan di bawah ini dilakukan dua perubahan yang terpisah:
(i) tekanan diturunkan pada suhu tetap;
(ii) suhu dinaikkan pada tekanan tetap.
Di antara reaksi kesetimbangan berikut, manakah yang menghasilkan kenaikan dalam jumlah produk ketika kedua perubahan di atas dilakukan adalah:
A. H2(g) + l2(g) ⇌ 2Hl(g) ;
B. 4NH3(g) + 5O2(g) ⇌ 4NO(g) + 6H2O(g);
C. N2(g) + 3H2(g) ⇌ 2NH3(g);
D. N2O4(g) ⇌ 2NO2(g);
E. CO(g) + H2O(g) ⇌ CO2(g) + H2(g);
Pembahasan Soal OSP Kimia 2018 Nomer 11
Dalam sistem kesetimbangan berlaku:
(i) tekanan diturunkan pada suhu tetap.
Jika tekanan diturunkan pada suhu tetap maka kesetimbangan akan bergeser ke arah jumlah zat (koefisien zat) terbesar.
Analisis:
Reaksi A, jumlah zat reaktan (2) = jumlah zat produk (2), tidak terjadi pergeseran
Reaksi B, jumlah zat reaktan (9) < jumlah zat produk (10), jumlah produk naik
Reaksi C, jumlah zat reaktan (4) > jumlah zat produk (2), jumlah produk turun
Reaksi D, jumlah zat reaktan (1) < jumlah zat produk (2), jumlah produk naik
Reaksi E, jumlah zat reaktan = jumlah zat produk, tidak terjadi pergeseran
(ii) suhu dinaikkan pada tekanan tetap
Jika suhu dinaikkan, kesetimbangan akan bergeser ke arah reaksi yang bersifat endoterm
Analisis:
Reaksi A ke kanan bersifat endoterm, jumlah produk naik
Reaksi B ke kanan bersifat eksoterm, jumlah produk turun
Reaksi C ke kanan bersifat eksoterm, jumlah produk turun
Reaksi D ke kanan bersifat endoterm, jumlah produk naik
Reaksi E ke kanan bersifat eksoterm, jumlah produk turun
Dari kedua perubahan, reaksi yang sanggup mengalami kenaikan jumlah produk ialah reaksi D.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 11 yang sempurna D
Soal OSP Kimia 2018 Nomer 12
Perhatikan reaksi kesetimbangan berikut:
CH3COOH(aq) ⇌ CH3COO–(aq) + H+(aq) + kalor
Pada ketika t1, sistem kesetimbangan mengalami gangguan ibarat plot pada grafik berikut:

Gangguan yang diberikan pada ketika t1 ialah sebagai akhir dari:
A. Penambahan HCI
B. Suhu diturunkan
C. Penambahan NaCH,COO
D. Penambahan CH,COOH
E. Volume wadah bertambah
Pembahasan Soal OSP Kimia 2018 Nomer 12
CH3COOH(aq) ⇌ CH3COO–(aq) + H+(aq) + kalor
Pada kurva/grafik tampak bahwa [H+] turun ketika t1. Ini berarti reaksi bergeser ke kiri, ke arah reaktan.
Analisis:
- Penambahan HCl berarti menambah [H+] yang ada di sisi produk reaksi memang akan meningkatkan jumlah reaktan, tetapi [H+] ini secara keseluruhan sanggup jadi tidak berkurang, alasannya ialah [H+] yang bereaksi dengan asetat akhir penambahan [H+] dari HCl.
- Reaksi ini bersifat eksoterm, reaksi akan bergeser ke reaktan bila suhu dinaikkan dan [H+] akan naik, tidak malah turun.
- Penambahan NaCH3COO, berarti menambah CH3COO– yang akan bereaksi dengan H+sehingga [H+] berkurang.
- Penambahan CH3COOH akan menyebabkan reaksi bergeser ke arah produk yang berarti akan menaikkan [H+]
- Volume wadah bertambah, maka reaksi akan ke arah produk yang memang mempunyai jumlah zat (lihat koefisien total) yang lebih besar. [H+] juga akan naik.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 12 yang sempurna C
Lanjut ke halaman selanjutnya
Soal OSP Kimia 2018 Nomer 13
Perbandingan volume yang harus dicampurkan antara larutan NH3 0,1 M (Kb= 2 x 10-5) dan HCI 0,1 M biar diperoleh larutan buffer yang mempunyai pH = 9 + log 3 adalah:
A. 2:3
B. 3:1
C. 3:5
D. 5:2
E. 5:3
Pembahasan Soal OSP Kimia 2018 Nomer 13
Kunci Jawaban Soal OSP Kimia 2018 Nomer 13 yang tepat
Soal OSP Kimia 2018 Nomer 14
Perhatikan kurva titrasi antara larutan asam lemah dengan larutan natrium hidroksida di bawah ini:

Perkiraan nilai pKa dari asam lemah tersebut adalah:
A. pKa = 2,7
B. pKa 4,5
C. pKa = 7,0
D. pKa = 9,5
E. pKa = 13,0
Pembahasan Soal OSP Kimia 2018 Nomer 14
Titrasi asam lemah dengan basa kuat, pada titik ekuivalen akan terbentuk garam terhidrolisis. Dari grafik tampak bahwa titik ekuivalen terjadi ketika pH = 9,5
pH = ½ (pKw + pKa + log [garam])
2 pH = pKw + pKa + log [garam]
2×9,5 = 14 + pKa + 0
19 = 14 + pKa
pKa = 19 – 14
pKa = 5
Perkiraan pKa yang paling mungkin dan mendekati ialah 4,5
Kunci Jawaban Soal OSP Kimia 2018 Nomer 14 yang sempurna B
Soal OSP Kimia 2018 Nomer 15
Jika 50,0 ml sampel larutan ammonium hidroksida dititrasi dengan asam sulfat:
2NH4OH(aq) + H2SO4(aq) →(NH4)2SO4(aq) + 2H2O(/)
untuk mencapai titik final dengan indikator metil merah, diperlukan 25,0 ml asam sulfat 0,200 M. Molaritas basa tersebut adalah:
A. 0,100M
B. 0,150M
C. 0,200 M
D. 0,300 M
E. 0,400 M
Pembahasan Soal OSP Kimia 2018 Nomer 15
Berdasarkan persamaan reaksi setara diketahui relasi sebagai berikut.
Jumlah NH4OH = 2 × jumlah H2SO4
50 mL × [NH4OH] = 2(25 mL × 0,2 M)
50 mL × [NH4OH] = 10 mmol
[NH4OH] = 10/50 M = 0,2 M
Kunci Jawaban Soal OSP Kimia 2018 Nomer 15 yang sempurna C
Soal OSP Kimia 2018 Nomer 16
larutan NaCl ditambahkan bertahap ke dalam larutan 0,010 M yang masing-masing mengandung ion Cu+“, Ag+, Au+ dan Tl+. Nilai Ksp masing-masing senyawa kloridanya berturut turut ialah 1,9×10-1, 1,6×10-10, 2,0×10-13 dan 1,9×10-4. Senyawa klorida yang akan mengendap pertama kali adalah:
A. CuCl(s)
B. AgCl(s)
C. AuCl(s)
D. TICl(s)
E. Semua mengendap pada ketika yang sama
Pembahasan Soal OSP Kimia 2018 Nomer 16
Pada soal diketahui bahwa semua mempunyai larutan sama dan bermuatan sama yaitu +1. Garam yang akan mengendap pertama kali ialah garam yang mempunyai nilai Ksp yang paling kecil (2×10–13), dalam hal ini AuCl(s)
Kunci Jawaban Soal OSP Kimia 2018 Nomer 16 yang sempurna C
Soal OSP Kimia 2018 Nomer 17
Di antara reaksi berikut ini yang sanggup diungkapkan dengan tetapan kesetimbangan basa, Kb, adalah:
A. [Zn(H2O)6]2+ ⇌ [Zn(H2O)5OH]+ + H+
B. CN– + H+ ⇌ HCN
C. F– + H2O ⇌ HF + OH–
D. Cr3+ + 6H2O ⇌ [Cr(H2O)6]3+
E. AlCl3 + H2O ⇌ Al(OH)3 + 3 HCl
Pembahasan Soal OSP Kimia 2018 Nomer 17
Kb adalah ungkapan untuk tetapan kesetimbangan basa lemah.
Basa lemah bila direaksikan dalam air akan menghasilkan OH–.
Reaksi:
F–(aq) + H2O(l) ⇌ HF(aq) + OH–(aq)
F– berperan sebagai basa
Kb = [HF][OH–]/[F–]
Kunci Jawaban Soal OSP Kimia 2018 Nomer 17 yang sempurna C
Soal OSP Kimia 2018 Nomer 18
Suatu sel elektrokimia terdiri dari elektroda perak dan elektroda emas yang masing-masing direndam dalam larutan Ag+ 1 M dan Au+ 1 M. Bila diketahui E0 Ag+IAg = +0,7991 V dan E0 Au+IAu = +1,68 V, maka potensial sel tersebut adalah:
A. -0,44 v
B. 0,00 v
C. +0,44 v
D. +0,88 v
E. +2,48 v
Pembahasan Soal OSP Kimia 2018 Nomer 18
Reaksi yang terjadi:
Ag + Au+ → Ag+ + Au
Jumlah elektron (n) yang terlibat dalam reaksi masing-masing 1 elektron
E0sel = E0 reduksi – E0 oksidasi
E0sel = (1,68 – 0,7991) volt
E0sel = 0,8809 volt
Potensial sel (Esel)
Esel = E0sel – 0,0592/n × log [Ag+]/[Au+]
Esel = 0,8809 – 0,0592/1 × log 1/1
Esel = 0,8809 – 0,0592 × log 1
Esel = 0,8809 – 0,0592 × 0
Esel = 0,8809 volt
Kunci Jawaban Soal OSP Kimia 2018 Nomer 18 yang sempurna D
Soal OSP Kimia 2018 Nomer 19
Selama elektrolisis air bahari dalam sel diafragma, dihasilkan gas klor, gas hidrogen dan natrium hidroksida. Rasio molar produk elektrolisis ini adalah:

Pembahasan Soal OSP Kimia 2018 Nomer 19
Rasio molar ialah perbandingan jumlah mol tiap spesi(zat) yang terlibat dalam reaksi. Rasio molar sanggup dilihat pada koefisien setiap zat dalam reaksi yang setara.
Air bahari mengandung ion Na+, Cl– dan H2O. Bila larutan tersebut dielektrolisis maka yang terjadi adalah:
2H2O(l) + 2e– → 2OH–(aq) + H2(g)
2Cl–(aq) → Cl2(g) + 2e–
2H2O(l) + 2Cl–(aq) → 2OH–(aq) + H2(g) + Cl2(g)
Reaksi lengkapnya:
2H2O(l) + 2NaCl(aq) → 2NaOH(aq) + H2(g) + Cl2(g)
jadi rasio molar Cl2 : H2 : NaOH = 1 : 1 : 2
Kunci Jawaban Soal OSP Kimia 2018 Nomer 19 yang sempurna B
Soal OSP Kimia 2018 Nomer 20
Perhatikan sel volta berikut ini:
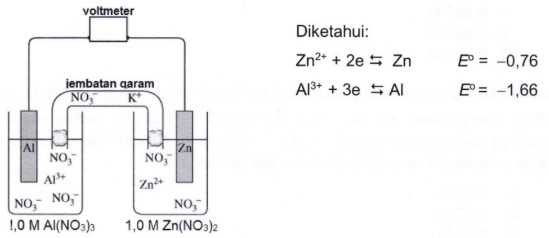
Jika sel volta tersebut digunakan, maka pernyataan yang benar adalah
A. Elektroda aluminium ialah katoda dan elektroda zink ialah anoda.
B. Elektron mengalir dari elektroda zink ke elektroda aluminium
C. Ion nitrat mengalir melalui jembatan garam ke larutan aluminium nitrat
D. Setengah reaksi yang terjadi di elektroda zink ialah Zn → Zn2+ + 2e–
E. Elektroda aluminium dan zink beratnya tetap
Pembahasan Soal OSP Kimia 2018 Nomer 20
Agar reaksi sanggup berlangsung maka Al harus mengalami oksidasi (Al(s) → Al3+ (aq) + 3e– ). Al melarut dan massanya berkurang.
Zn harus mengalami reduksi (Zn2+(aq) + 2e– → Zn(s)). Zn massanya akan bertambah.
Oksidasi terjadi di anode, Al berperan sebagai anode. Reduksi terjadi di katoda, Zn berperan sebagai katoda.
Aliran elektron dari anode Al daerah elektron dilepaskan menuju katode Zn.
Karena Al3+ jumlahnya bertambah selama reaksi maka akan dinetralkan dengan ion nitrat yang mengalir melalui jembatan garam. Ion nitrat mengalir ke larutan Al(NO3)3.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 20 yang sempurna C
Soal OSP Kimia 2018 Nomer 21
Suatu senyawa kromium dengan rumus umum CrCl3.6H2O , bila dilarutkan dalam air membentuk ion kompleks dengan ion Cl– dan H2O bertindak sebagai ligan. Jika larutan ini direaksikan dengan larutan AgNO, berlebih, hanya sepertiga dari total ion klorida yang diendapkan sebagai AgCI. Rumus kimia ion kompleks dari Cr3+ ini dalam larutan tersebut ialah …
A. Cr3+‘(aq)
B. [Cr(H2O)6]3+
C. [Cr(H2O)5CI]2+
D. [Cr(H2O)4Cl2]+
E. [Cr(H2O)3CI3]
Pembahasan Soal OSP Kimia 2018 Nomer 21
Pada soal dinyatakan bahwa hanya sepertiga dari total ion klorida yang sanggup diendapkan sebagai AgCl. Kata sepertiga boleh diartikan 1 dari 3 ion Cl yang ada dalam senyawa yang akan bereaksi dengan Ag+ membentuk AgCl dan masih ada 2 ion Cl dalam senyawa tersebut.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 21 yang sempurna D
Soal OSP Kimia 2018 Nomer 22
Urutan kereaktifan 3 senyawa berikut terhadap reaksi yang mengikuti prosedur SN2 adalah …

A. A>B>C
B. A> C> B
C. B >A> C
D. B > C >A
E. C >A> B
Pembahasan Soal OSP Kimia 2018 Nomer 22
Urutan kereaktifan senyawa dalam reaksi yang mengikuti meknisme SN2 ialah senyawa yang sedikit mempunyai halangan sterik akan lebih reaktif dibanding yang lebih banyak halangan sterik.
Dalam hal ini B kurang terhalang dan lebih reaktif dibandingkan C dan A yang paling banyak halangan steriknya.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 22 yang sempurna D
Soal OSP Kimia 2018 Nomer 23
Di antara reagen berikut yang sanggup mengubah sikloheksena menjadi cis-glikol adalah:
A. natrium terl-butoksida dalam kloroform
B. hidrogen peroksida dan larutan asam asetat
C. ozon dan serbuk seng dalam sedikit air
D. asam periodat
E. larutan encer kalium permanganat dingin
Pembahasan Soal OSP Kimia 2018 Nomer 23
Glikol atau diol ialah senyawa kimia yang mengandung dua gugus hidroksil (OH).
Dari siklohekena (suatu alkena) berkembang menjadi cis-glikol melalui reaksi oksidasi.
Tentu saja memakai zat yang sanggup mengoksidasi sikloheksena.Oksidator yang paling mungkin ialah larutan encer KMnO4 dingin, OH– atau NaOH.
Reaksi singkat:
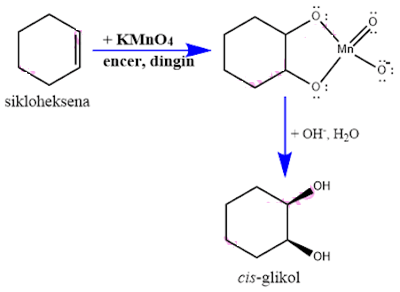
Kunci Jawaban Soal OSP Kimia 2018 Nomer 23 yang sempurna E
Soal OSP Kimia 2018 Nomer 24
Hubungan antara kedua senyawa di bawah ini:
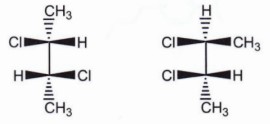
Adalah
A. Enantiomer
B. Diastereomer
C. Isomer geometri
D. Isomer struktur
E. Senyawa yang sama namun berbeda konformasi
Pembahasan Soal OSP Kimia 2018 Nomer 24
Lakukan analisis putaran gugus fungsi prioritas. Gugus fungsi cabang nomor tertinggi menerima prioritas.
Karena ada 2 sentra C kiral maka harus dicek keduanya apakah mengikuti putaran R (searah jarum jam) atau S (berlawanan arah jarum jam). Untuk pembahasan mengenai hal ini sanggup dipelajari detilnya di sini.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 24 yang sempurna A
Soal OSP Kimia 2018 Nomer 25
Konformasi Newman yang sempurna untuk senyawa 2-metil siklopentanon bila dilihat dari posisi atom C1 dan C2 adalah:
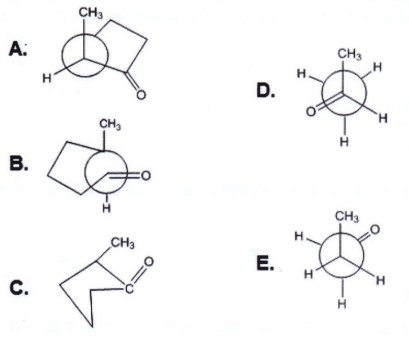
Pembahasan Soal OSP Kimia 2018 Nomer 25
Jika dilihat posisi atom C1 ke C2, maka posisi C1 yang mengikat atom O berada sempurna di depan mata, di depat bulatan, dan posisi C2 yang mengikat CH3 di belakang.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 25 yang sempurna B
Soal OSP Kimia 2018 Nomer 26
Di antara senyawa berikut yang merupakan produk dari sketsa reaksi berikut:

A. I
B. Il
C. III
D. IV
E. V
Pembahasan Soal OSP Kimia 2018 Nomer 26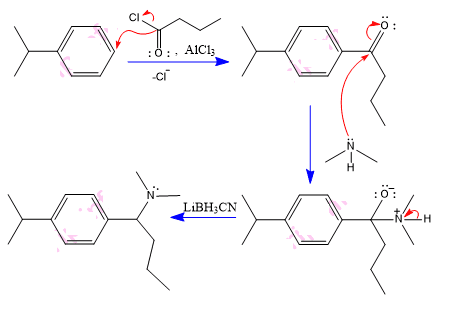
Kunci Jawaban Soal OSP Kimia 2018 Nomer 26 yang sempurna C
Soal OSP Kimia 2018 Nomer 27
Jika senyawa 4-fenil-1-butena di bawah ini direaksikan dengan Cl2. UV, maka produk utama yang akan dihasilkan adalah:
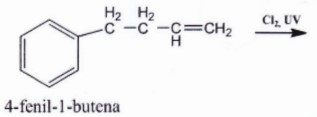
A. 4-fenil-3- kloro-1- butena
B. 4-fenil-4- kloro-1- butena
C. 4-fenil-1- kloro-1-butena
D. 4-feniil-2- kloro-1-butena
E. 4-fenil-1,2- diklorobutana
Pembahasan Soal OSP Kimia 2018 Nomer 27
Ini merupakan reaksi adisi, yang diawali dengan pembelahan Cl-Cl menjadi radikal bebas dengan adanya sinar UV.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 27 yang sempurna E
Soal OSP Kimia 2018 Nomer 28
Perhatikan rangkaian reaksi berikut:
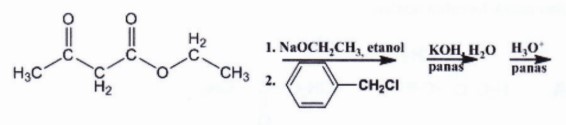
Produk final dari rangkaian reaksi di atas adalah:

Pembahasan Soal OSP Kimia 2018 Nomer 28
Mekanisme yang terjadi:
1) Reaksi asam-basa;
2) Reaksi alkilasi;
3) Reaksi hidrolisis ester;
4) Reaksi Dekarboksilasi
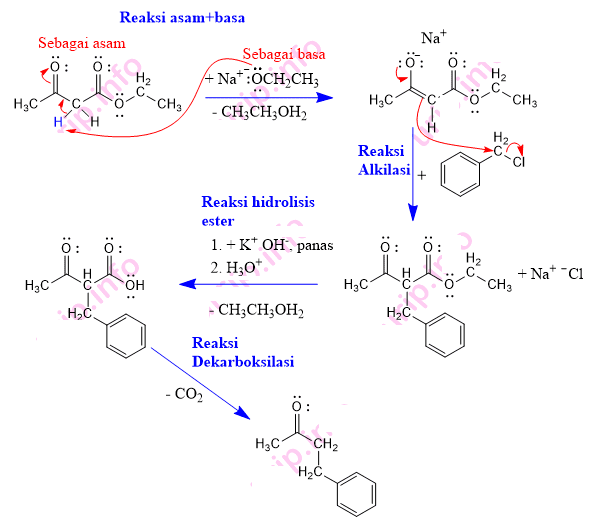 Tentang prosedur reaksi hidrolisis ester oleh basa sanggup dipelajari secara lengkap, silakan baca di sini.
Tentang prosedur reaksi hidrolisis ester oleh basa sanggup dipelajari secara lengkap, silakan baca di sini.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 28 yang sempurna E
Soal OSP Kimia 2018 Nomer 29
Pereaksi yang paling sempurna untuk reaksi berikut

adalah:
A. HCO2CH2C6H5
B. C6H5CH2COOH
C. C6H5CH2CI
D. C6H5CHCICOOH
E. O=C(CH2C6H5)2
Pembahasan Soal OSP Kimia 2018 Nomer 29
Untuk memilih reaktan sanggup ditelusuri setahap demi setahap ibarat berikut:
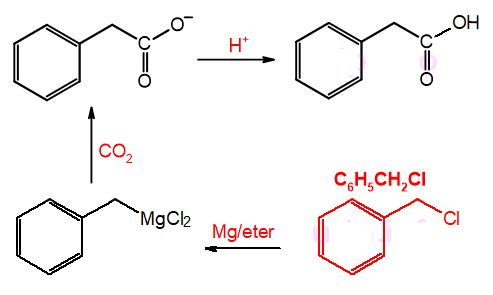
Kunci Jawaban Soal OSP Kimia 2018 Nomer 29 yang sempurna C
Soal OSP Kimia 2018 Nomer 30
Perhatikan reaksi ozonolisis berikut ini:

Produk dari reaksi tersebut adalah:
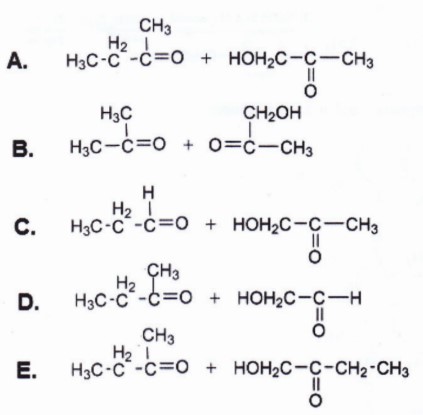
Pembahasan Soal OSP Kimia 2018 Nomer 30
Reaksi ozonolisis 2,3-dimetil-2-pentena-1-ol secara singkat sanggup ditulis:
Kunci Jawaban Soal OSP Kimia 2018 Nomer 30 yang sempurna A
Keyword : Soal OSP 2018, Soal OSP Kimia 2018, Download Soal OSP 2018, Download Soal OSP Kimia 2018, Soal dan Kunci Jawaban OSP 2018, Soal dan Kunci Jawaban OSP Kimia 2018, Pembahasan Soal OSP 2018, Pembahasan Soal OSP Kimia 2019, Soal Kimia OSP 2018, Download Soal Kimia OSP 2018, Soal dan Kunci Jawaban Kimia OSP 2018, Pembahasan Soal Kimia OSP 2018
Demikian tadi isu terbaru mengenai Download Soal dan Pembahasan OSP Kimia 2018 PDF semoga bermanfaat untuk menunjang prestasi akademik di OSN 2019.
Download Soal dan Pembahasan OSP Kimia 2018 PDF DOC
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon