Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 1-10 – Dalam mempersiapkan seleksi Olimpiade Sains Nasional tingkat Provinsi (OSP) tahun 2019, perlu adanya pembahasan soal OSP 2018. Untuk mapel Kimia, berikut ini ialah pembahasan soal OSP Kimia tahun 2018 PDF klik logo print.Ke depan aku sediakan Pembahasan Soal OSP Kimia 2019.
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 1-10
Soal OSP Kimia 2018 Nomer 1 PDF DOC rukim.id
Brom (Br2) diekstrak dari Laut Mati (Dead Sea), ditransportasikan sebagai larutan 52% massa kalsium bromida. Massa brom (dalam ton) yang terkandung dalam 100 ton larutan ini ialah …
A. 15,6 ton
B. 20,8 ton
C. 29,4 ton
D. 41,6 ton
E. 52,0 ton
Pembahasan Soal OSP Kimia 2018 Nomer 1 PDF DOC
Massa molar CaBr2 = (40,08 + 79,90×2) g/mol
Massa molar CaBr2 = 199,88 g/mol
Massa molar Br2 = (79,90×2) g/mol
Massa molar Br2 = 159,80 g/mol
Dengan kadar 52% CaBr2 sebanyak 100 ton larutan terdapat 52 ton CaBr2.
52 ton = 52 × 106 gram
Br2 diekstrak berdasar reaksi:
CaBr2 → Ca2+ + Br2
Dari persamaan reaksi diketahui bahwa setiap jumlah (mol) CaBr2 setara dengan jumlah (mol) Br2
52 ton CaBr2 = 52×106 g / 199,88 g/mol
52 ton CaBr2 = 260.156,09 mol
Jumlah Br2 = jumlah CaBr2
Jumlah Br2 = 260.156,09 mol
Jumlah Br2 = 260.156,09 mol×159,80 g/mol
Jumlah Br2 = 41.572.943,18 g
Jumlah Br2 = 41.572.943,18 g106 g/ton
Jumlah Br2 = 41,572943 ton=41,60 ton
Kunci Jawaban Soal OSP Kimia 2018 Nomer 1 yang sempurna D.
Soal OSP Kimia 2018 Nomer 2 PDF DOC rukim.id
Magnesium sebanyak 2,4 g dimasukkan ke dalam 350 ml larutan HCI 1,0 M. Setelah reaksi selesai, MgCl2 yang terbentuk sebanyak 4,75 gram. Persen hasil MgCI2 adalah:
A. 25
B. 50
C. 75
D. 90
E. 100
Pembahasan Soal OSP Kimia 2018 Nomer 2 PDF DOC
Massa molar Mg = 24,31 g/mol
Massa molar MgCl2 = (24,31 + 35,45×2) g/mol
Massa molar MgCl2 = 95,21 g/mol
Reaksi yang terjadi:
Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
Hitungan stoikiometris:
2,4 g Mg = 2,4 g ÷ 24,31 g/mol
2,4 g Mg = 0,10 mol
350 mL HCl 1 M = 0,35 l × 1 M
350 mL HCl 1 M = 0,35 mol
Secara teori massa MgCl2 seharusnya adalah
0,1 mol × 95,21 g/mol = 9,521 g
Kadar MgCl2 = (massa positif ÷ massa teori) × 100%
Kadar MgCl2 = (4,75 ÷ 9,521) × 100%
Kadar MgCl2 = 49,89% ≈ 50%
Kunci Jawaban Soal OSP Kimia 2018 Nomer 2 yang sempurna B
Soal OSP Kimia 2018 Nomer 3 PDF DOC rukim.id
Nitrogliserin, suatu materi peledak, terurai sesuai persamaan berikut:
4C3H5(NO3)3(s) → 12CO2(g) + 10H2O(g) + 6N2(g) + O2(g)
Jika 260 g nitrogliserin terurai, maka volume gas yang dihasilkan pada tekanan 1,2 atm dan 270C adalah:
A. 41 L
B. 105 L
C. 130 L
D. 170 L
E. 235 L
Pembahasan Soal OSP Kimia 2018 Nomer 3 PDF DOC
Massa molar C3H5(NO3)3 = 227,09 g/mol
260 g C3H5(NO3)3 = 260 g ÷ 227,09 g/mol
260 g C3H5(NO3)3 = 1,145 mol
Semua hasil reaksi berupa gas dengan total koefisien gas = 12+10+6+1=29
Berdasarkan perbandingan koefisien zat pada persamaan reaksi setara maka
jumlah gas hasil (mol) = 29 × (jumlah C3H5(NO3)3 ÷ 4)
jumlah gas hasil (mol) = 29 × (1,145 mol ÷ 4)
jumlah gas hasil (mol) = 8,30125 mol
Volume gas pada tekanan 1,2 atm dan temperatur 27 oC (= 300 K) sanggup dihitung dengan rumus:
V = (n.R.T) ÷ P
V = (8,30125 mol × 0,08205 L.atm/K.mol × 300 K) ÷ 1,2 atm
V = 170,279390625 L ≈ 170 L
Kunci Jawaban Soal OSP Kimia 2018 Nomer 3 yang sempurna D
Soal OSP Kimia 2018 Nomer 4 PDF DOC
Tekanan osmosis sanggup dipakai untuk memilih berat molekul suatu senyawa dan umumnya dipakai untuk menghitung massa molekul protein. Jika 1,00 g protein dilarutkan dalam 100 ml air, tekanan osmosisnya menjadi 92,90 mm Hg. Massa molekul protein tersebut ialah (asumsi: i = 1 dan suhu 250C):
A. 100
B. 400
C. 1000
D. 2000
E. 4000
Pembahasan Soal OSP Kimia 2018 Nomer 4 PDF DOC
Tekanan osmosis (p)
p = (n/V) × R × T × i
p × V = n × R × T × 1
p × V = massa protein/massa molar protein × R × T
p × V × massa molar protein = massa protein × R × T
massa molar protein = massa protein×R×T / π×V
massa molar protein = 1 g x 0,08205 × 298 / 92,90/760 atm × 100/1000 L
massa molar protein = 24,45090 / 0,0122237 g/mol
massa molar protein = 2000 g/mol
Jadi massa molekul relatif protein tersebut ialah 2000
Kunci Jawaban Soal OSP Kimia 2018 Nomer 4 yang sempurna D
Soal OSP Kimia 2018 Nomer 5 PDF DOC
Gallium mempunyai konfigurasi elektron [Ar] 3d10 4s24 p1, dengan [Ar] mewakili konfigurasi elektron argon. Urutan pelepasan elektron yang sempurna untuk membentuk ion G4+ adalah:

Pembahasan Soal OSP Kimia 2018 Nomer 5 PDF DOC
Konfigurasi elektron Ga = [Ar] 3d104s24p1
Elektron yang akan terionkan lebih dahulu ialah elektron pada kulit terluar, dalam hal ini ialah kulit ke-4, lalu gres kulit ke-3. 4p ialah mempunyai energi relatif lebih tinggi dibanding 4s.
Oleh alasannya ialah itu urutan pelepasan elektronnya di mulai dari 4p, 4s, 4s, 3d
Kunci Jawaban Soal OSP Kimia 2018 Nomer 5 yang sempurna E
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 1-10
Soal OSP Kimia 2018 Nomer 6 PDF DOC
Di antara pasangan molekul berikut ini, yang mengatakan bahwa dipol permanen dalam molekul I lebih besar dibandingkan dalam molekul II adalah:
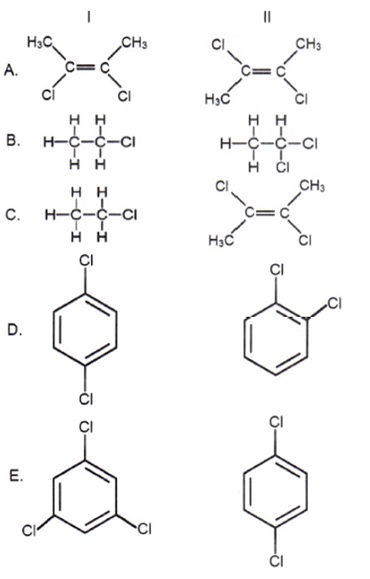
Pembahasan Soal OSP Kimia 2018 Nomer 6 PDF DOC
Dipol permanen terjadi alasannya ialah adanya ikatan atau gaya tarik antara 2 atom yang mempunyai perbedaan keelektronegatifan yang signifikan, dipol permanen terjadi pada molekul yang bersifat polar.
Selain itu geometri molekul (posisi atom-atom dalam molekul) juga memilih kepolaran secara keseluruhan.
Bila resultan gaya tarik dalam molekul saling meniadakan (simetris) maka menghasilkan molekul yang nonpolar atau kurang polar, sedangkan bentuk molekul yang asimetris relatif lebih polar.
Berikut ini kesimpulan wacana dipol permanen yang dibandingkan:
- I > II
- I < II
- I > II
- I < II
- Gugus Cl pada kedua molekul menghasilkan resultan nol
Kunci Jawaban Soal OSP Kimia 2018 Nomer 6 yang sempurna A dan C
Soal OSP Kimia 2018 Nomer 7 PDF DOC
Berdasarkan struktur senyawa berikut ini:
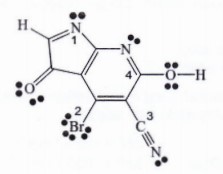
Jumlah ikatan sigma (σ) dan pi (π) dalam struktur senyawa tersebut masing masing adalah:
A. 10 ikatan σ dan 13 ikatan π
B. 13 ikatan σ dan 13 ikatan π
C. 15 ikatan σ dan 6 ikatan π
D. 16 ikatan σ dan 6 ikatan π
E. 17 ikatan σ dan 7 ikatan π
Pembahasan Soal OSP Kimia 2018 Nomer 7 PDF DOC
Setiap ikatan tunggal merupakan ikatan
Setiap ikatan rangkap dua, terdiri dari 1 ikatan dan 1 ikatan
Setiap ikatan rangkap tiga, terdiri dari 1 ikatan dan 2 ikatan
Dalam struktur molekul dalam soal terdiri:
11 ikatan tunggal = 11 ikatan
5 ikatan rangkap dua = 5 ikatan dan 5 ikatan
1 ikatan rangkap tiga = 1 ikatan dan 2 ikatan
Jadi secara keseluruhan dalam molekul terdapat 17 ikatan dan 7 ikatan
Kunci Jawaban Soal OSP Kimia 2018 Nomer 7 yang sempurna E
Soal OSP Kimia 2018 Nomer 8 PDF DOC
Sejak tahun 1850, sebagian besar buku dicetak pada kertas asam yang mengakibatkan buku menjadi ringkih dan cepat rusak alasannya ialah mengandung residu asam dan sedikit air yang tertahan di kertas tersebut. Untuk mencegahnya, buku diawetkan dengan mereaksikan kertas dan uap dietilzink, Zn(C2H5)2. Reaksi dietilzink dengan suatu asam HX menghasilkan etana:
Zn(C2H5)2 + 2HX → ZnX2 + 2C2H6.
Produk yang dihasilkan dari reaksi antara dietilzink dengan air adalah:
A. ZnH2 dan C2H6
B. ZnH2 dan C2H5OH
C. Zn(OH)2 dan C2H6
D. Zn(OH)2 dan C2H5OH
E. Zn dan C2H6
Pembahasan Soal OSP Kimia 2018 Nomer 8 PDF DOC
Reaksi antara dietilzink dengan air ini seolah-olah dengan reaksi yang diberikan pada soal. H–X tipenya seolah-olah H–OH. Pada HX, X– yang berikatan dengan Zn2+, kalau dengan air maka Zn2+ yang berikatan ialah OH–. Sementara itu etil akan berikatan dengan H membentuk etana (C2H6)
Reaksi yang terjadi:
Zn(C2H5)2 + H2O → Zn(OH)2 + 2C2H6
Kunci Jawaban Soal OSP Kimia 2018 Nomer 8 yang sempurna C
Soal OSP Kimia 2018 Nomer 9 PDF DOC
Reaksi 3O2 → 2O3 berlangsung dengan laju hilangnya O2 setara dengan 0,60 mol/L.det. Besar laju terbentuknya O3 (dalam mol/L.det) adalah:
A. 1,20
B. 0,90
C. 0,60
D. 0,40
E. 0,10
Pembahasan Soal OSP Kimia 2018 Nomer 9 PDF DOC
Reaksi yang terjadi:
3O2 → 2O3
−rO2 = 0,6mol/L
Tanda + dan – hanya dipakai untuk menandai bahwa zat bertambah atau berkurang saja.
Pernyataan laju reaksi di atas sanggup ditulis:
Kunci Jawaban Soal OSP Kimia 2018 Nomer 9 yang sempurna D
Soal OSP Kimia 2018 Nomer 10 PDF DOC
Reaksi 2C4H6 → C8H12, aturan lajunya ialah r = k[C4H6]2. Jika [C4H6] = 2,0 M, laju reaksinya ialah 0,106 M/det. Jika [C4H6] = 4,0 M, maka laju reaksinya adalah:
A. 0,022M/det
B. 0,053 M/det
C. 0, 106 M/det
0. 0,212 M/det
E. 0,424 M/det.
Pembahasan Soal OSP Kimia 2018 Nomer 10 PDF DOC
2C4H6 → C8H12
r = k [C4H6]2
Jika [C4H6] = 2 M → r = 0,106 M/det
k = r ÷ [C4H6]2
k = 0,106 M/det ÷ (2 M)2
k = 0,106 M/det ÷ 4 M2
Jika [C4H6] = 4 M
r = k [C4H6]2
r = (0,106 M/det ÷ 4 M2) × (4 M)2
r = (0,106 M/det ÷ 4 M2) × 16 M2
r = 0,106 M/det × 4 M2
r = 0,424 M/det
Kunci Jawaban Soal OSP Kimia 2018 Nomer 10 yang sempurna E
Demikian tadi pembahasan soal OSP Kimia tahun 2018 untuk nomor 1-10. Nomor yang lain menyusul.
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 1-10
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 11-20
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 21-30
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 1-10
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon