Download Pembahasan Soal OSP Kimia 2015 Nomor 11 hingga 20 – Dalam mempersiapkan OSP Kimia tahun 2017 2018 2019 2020 dan OSP tahun-tahun yang akan datang, maka perlu adanya pembahasan soal OSP Kimia tahun sebelumnya. Kali ini akan ada pembahasan soal Kimia Olimpiade Sains Nasional tingkat Provinsi tahun 2015. Pembahasan kali ini khusus Pilihan Ganda (Pilgan). Saya buat beberapa halaman, semoga membacanya tidak terlalu ke bawah.
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 11 – 20
Download PDF DOC | Soal OSP Kimia 2015 Nomor 11
Perhatikanlah reaksi pembentukan glukosa (C6H12O6) berikut ini:
CO2(g) + 2C2H5OH(l) + energi panas ⇌ C6H12O6(aq)
Berikut ini, manakah pernyataan yang benar mengenai persen hasil C6H12O6?
A. Persen hasil C6H12O6 bertambah besar jikalau tekanan parsial CO2 diturunkan.
B. Persen hasil C6H12O6 naik dua kali jikalau tekanan parsial CO2 diduakalikan
C. Persen hasil C6H12O6 bertambah besar jikalau jika suhu dinaikkan
D. Persen hasil C6H12O6 berkurang jikalau suhu diturunkan
E. Persen hasil C6H12O6 berkurang jikalau bila tekanan total sistem reaksi dinaikkan
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 11
Reaksi pada soal ini ialah reaksi bersifat endoterm, reaksi yang sanggup berlangsung jikalau tersedia cukup energi. Ketika suhu dinaikkan tentu saja persen hasil C6H12O6 bertambah besar dibanding kondisi sebelumnya. Namun jikalau suhu diturunkan pada sistem kesetimbangan maka persen hasil C6H12O6 otomatis akan mengalami pengurangan. Jada balasan C dan D sanggup dimaknai sama.
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 11 (C dan D)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 12
Di dalam reaksi kimia perubahan senyawa X menjadi senyawa Z, melalui mekanismenya ditemukan bahwa langkah reaksi berlangsung melalui pembentukan senyawa Y, yang sanggup diisolasi. Tahap yang dilalui adalah:
X → Y, ∆H = positif
Y → Z, ∆H = negatif.
Berdasarkan isu tersebut, manakah profil energi pada reaksi yang sesuai dengan data ini?
Download PDF DOC | Pembahasan Soal OSP Kimia Nomor 12
X → Y, ∆H = positif → energi Y > X maka akan bersifat endoterm
Y → Z, ∆H = negatif → energi Z < Y maka akan bersifat eksoterm
Karena Y sanggup diisolasi maka posisi Y pada profil energi harus berada pada cenkungan (lembah).
Download PDF DOC | Kunci Jawaban Soal OSP Kimia Nomor 12 (A)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 13
Perhatikan reaksi gas pencemar NO2 dan ozon berikut ini: 2NO2 (g) + O3(g) ⇌ N2O5 (g) + O2 (g)
Reaksi tersebut diamati lajunya dan diperoleh data berikut ini:
Dari percobaan tersebut, manakah pernyataan yang benar mengenai aturan laju reaksinya (r):
A. r = k[NO2]2 [O3]
B. r = k[NO2] [O3]2
C. r = k[NO2] [O3]
D. r = k[NO2]
E. r = k [O3]
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 13
Untuk memilih laju reaksi diharapkan orde reaksi setiap pereaksi dengan memanfaatkan data percobaan.
Orde reaksi terhadap NO2 dapat dipakai data O3 yang konsentrasinya tetap, dalam hal ini sanggup memakai data percobaan 2 dan 1.
(0,0022/0,0015)x = (7,2×10–8)/(4,8×10–8)
(1,47)x = 1,50 → ( 1,5)x = 1,50 → x = 1
Orde reaksi terhadap O3 dapat dipakai data NO2 yang konsentrasinya tetap, dalam hal ini sanggup memakai data percobaan 3 dan 2 .
(0,005/0,0025)y = (1,4×10–7)/(7,2×10–8)
2y = 1,94 → 2y = 2 → y = 1
Jadi persamaan laju reaksi r = k[NO2] [O3]
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 13 (C)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 14
Reaksi berikut ini, 3ClO–(aq) →ClO3– (aq) + 2Cl– (aq) telah diusulkan berlangsung melaui prosedur berikut ini:
ClO– (aq) + ClO– (aq)→ ClO2– (aq) + Cl– (aq) (lambat)
ClO2– (aq) + ClO– (aq) → ClO3– (aq) + Cl– (aq) (cepat)
Hukum laju manakah yang konsisten dengan prosedur ini?
A. laju = k[ClO–]2
B. laju = k[ClO–]
C. laju = k[ClO2–][ClO–]
D. laju = k[Cl–][ClO–]2
E. laju = k[ClO3–][Cl–]
F. Hukum laju harus ditetentukan secara eksperimen, bukan dari stoikiometri.
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 14
Umumnya laju reaksi ditentukan pada tahap lambat, meskipun laju reaksi memang harus ditentukan secara eksperimen dan bukan dari stoikiometri. Pada tahap lambat menyerupai pada soal ini ditentukan menurut stoikiometeri tahap lambar sehingga balasan A lebih sempurna dibanding B, C, D, dan E. Pada soal ini Sebenarnya alternatif hanya hingga E, F tidak ada namun pada kunci balasan diberikan alternatif begitu.
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 14 (A)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 15
Kesetimbangan berikut terjadi dalam adonan asam nitrat pekat dan asam sulfat pekat.
HNO3 + 2H2SO4 ⇌ NO2+ + 2HSO4– + H3O+.
Pernyataan manakah perihal kesetimbangan ini yang benar ?
A. Penambahan H2O akan mengurangi konsentrasi NO2+
B. HNO3 dan NO2+ adalah pasangan asam-basa konjugasi
C. Asam nitrat bertindak sebagai suatu oksidator
D. Asam sulfat bertindak sebagai dehidratator
E. Asam sulfat bertindak sebagai suatu basa
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 15
Reaksi pada soal ini bukanlah reaksi redoks, bilangan oksidasi atom tidak ada yang berubah. Penambahan air berarti menawarkan dampak pengenceran sehingga konsentrasi NO2+ berkurang. HNO3 bertindak sebagai suatu basa dengan kehadiran H2SO4 yang merupakan asam yang lebih kuat, ini menjadikan asam nitrat terionisasi menjadi HO– dan +NO2 (biasanya kalau HNO3berperan sebagai asam terionkan menjadi H+ dan –ONO2 atau NO3–)
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 15 (A)
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 11 – 20
Download PDF DOC | Soal OSP Kimia 2015 Nomor 16
Konstanta kesetimbangan reaksi berikut ini masing masing adalah K1, K2, dan K3.
| HNO2(aq) + H2O(l) ⇌ NO2−(aq) + H3O+(aq) | K1 |
| 2H2O(l) ⇌ H3O+(aq) + OH−(aq) | K2 |
| NH3(aq) + H2O(I) ⇌ NH4(aq) + OH(aq) | K3 |
Bagaimana konstanta kesetimbangan untuk reaksi dibawah ini?
HNO2(aq) + NH3(aq) ⇌ NO2−(aq) + NH4(aq)
A. K1 – K2 + K3
B. K1 K3
C. K1 K3 / K2
D. K1 K2 K3
E. K2 / (K1 K3)
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 16
Fokus pada persamaan yang akan ditentukan nilai K-nya:
HNO2(aq) + NH3(aq) ⇌ NO2−(aq) + NH4(aq)
Pastikan spesi-spesi yang ada di ruas kiri dan kanan sesuai persamaan reaksi itu dengan membalik atau menempatkan spesi yang diketahui nilai K1 atau K2 atau K3.
| HNO2(aq) + H2O(l) ⇌ NO2−(aq) + H3O+(aq) | K1 |
| H3O+(aq) + OH−(aq) ⇌ 2H2O(l) | 1/K2 |
| NH3(aq) + H2O(l) ⇌ NH4(aq) + OH(aq) | K3 + |
| HNO2(aq) + NH3(aq) ⇌ NO2−(aq) + NH4(aq) | (K1.K3)/K2 |
Ingat membalik persamaan reaksi maka nilai K-nya ialah menjadi 1/K; menjumlahkan persamaan reaksi maka K-nya ialah hasil kali nilai K dari masing-masing persamaan reaksi.
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 16 (C)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 17
Setengah reaksi yang terjadi di anoda pada reaksi setara dibawah ini:
3MnO4–(aq) + 24H+(aq) + 5Fe(s) → 3Mn2+(aq) + 5Fe3+(aq) + 12H2O (l)
adalah:
A. 2MnO4–(aq) + 12H+(aq) + 6e– → 2 Mn2+(aq) + 3H2O (l)
B. MnO4–(aq) + 8H+(aq) + 5e– → Mn2+(aq) + 4H2O (l)
C. Fe(s) → Fe3+(aq) + 3e–
D. Fe2+(aq) → Fe3+ (aq) + e–
E. Fe(s) → Fe2+(aq) + 2e–
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 17
Reaksi yang terjadi di anoda ialah reaksi oksidasi, di katoda ialah reaksi reduksi.
Sesuai persamaan reaksi redoks yang terjadi yang mengalami oksidasi ialah Fe (s) menjelma Fe3+(aq).
Fe(s) → Fe3+(aq) + 3e–
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 17 (C)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 18
Perhatikan sel volta berikut ini: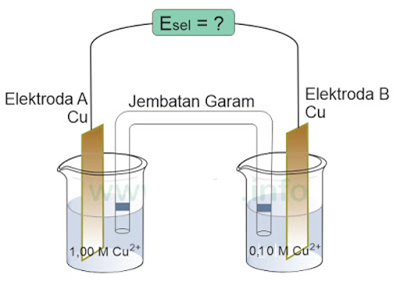
Cu2+ (aq) + 2e– → Cu(s) E° = 0,340 V
Berapakah potensial sel volta ini, Esel?
A. +0,0296
B. -0,0370 V
C. +0,0592 V
D. -0,399 V
E. 0 V
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 18
Soal ini sanggup diselesaikan dengan memakai persamaan Nernst
Cu(s) | Cu2+ (0,1 M) || Cu2+ (1,0 M) | Cu(s)
Esel=Eosel−0,0592nlog[oksidasi][reduksi]
Esel=0−0,05922log0,1 M1,0 M
Esel=0−0,05922×(−1)
Esel=0+0,05922
Esel=+0,0296
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 18 (A)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 19
Bagaimana bentuk geometri, bilangan oksidasi, bilangan koordinasi tembaga, untuk ion kompleks, [Cu(NH3)4(OH2)2]2+?
A. tetrahedral ; +2 ; 6
B. square planar ; -2 ;4
C. oktahedral ; +2 ;6
D. linear ; +3; 2
E. trigonal planar ; +1; 4
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 19
[Cu(NH3)4(OH2)2]2+
Jika diuraikan maka akan terdapat 6 buah ligan yaitu 4NH3 dan 2H2O keduanya netral, jadi muatan 2+ itu berasal dari Cu2+
Ion kompleks dengan 6 buah ligan akan membentuk geometri oktahedral, bilangan oksidasinya sesuai muatan Cu yaitu +2, bilangan koordinasi Cu sesuai jumlah ligan yang terikat yaitu 6.
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 19 (C)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 20
Mengenai garam kompleks [Co(NH3)5Cl]Cl2, manakah pernyataan yang tidak sempurna :
A. Larut dalam air
B. Dapat menghantarkan listrik.
C. Larutan 1 mol [Co(NH3)5Cl]Cl2menghasilkan 1 mol kation dan 3 mol anion.
D. Dalam air, kation kompleks yang terbentuk ialah [Co(NH3)5Cl]2+
E. Mengandung ligand NH3 dan Cl–.
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 20
Umumnya larutan garam kompleks larut dalam air, sanggup menghantarkan listrik.
[Co(NH3)5Cl]Cl2 → NH3 dan Cl– itu ialah ligan
Dalam air [Co(NH3)5Cl]Cl2 → [Co(NH3)5Cl]2+ + 2Cl–
Jadi setiap 1 mol [Co(NH3)5Cl]Cl2 menghasilkan 1 mol kation dan 2 mol anion
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 20 (C)
Demikian tadi pembahasan soal Kimia OSP 2015 untuk nomor 11 hingga 20. Untuk nomor selanjutnya sanggup di saluran melalui link di bawah ini.
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 1 – 10
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 11 – 20
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 21 – 30
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 11 – 20
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon