Download Pembahasan Soal OSP Kimia 2015 Nomor 1 sampai 10 – Dalam mempersiapkan OSP Kimia tahun 2017 2018 2019 2020 dan OSP tahun-tahun yang akan datang, maka perlu adanya pembahasan soal OSP Kimia tahun sebelumnya. Kali ini akan ada pembahasan soal Kimia Olimpiade Sains Nasional tingkat Provinsi tahun 2015. Pembahasan kali ini khusus Pilihan Ganda (Pilgan). Saya buat beberapa halaman, biar membacanya tidak terlalu ke bawah.
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 1 – 10
Download PDF DOC | Soal OSP Kimia 2015 Nomor 1
Bila Cu(CN)2 dipanaskan, dihasilkan C2N2(sianogen) dan CuCN. Berapa massa Cu(CN)2dibutuhkan untuk menciptakan C2N2 sebanyak 5,00 g? (Mr Cu(CN)2 = 115,6; C2N2 = 52,04)
A. 20,2 g
B. 22,2 g
C. 24,2 g
D. 26,4 g
E. 28,6 g
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 1
Reaksi pemanasan setara: 2Cu(CN)2 → C2N2 + 2CuCN
Jumlah C2N2 = 5 g/52,04 g/mol = 0,09608 mol
Jumlah Cu(CN)2 = 2 × jumlah C2N2
Jumlah Cu(CN)2 = 2 × 0,09608 mol
Jumlah Cu(CN)2 = 0,19216 mol
Jadi massa Cu(CN)2 yang diharapkan = 0,19216 mol × 115,6 g/mol
Jadi massa Cu(CN)2 yang dibutuhkan = 22,21368 g ≈ 22,2 g
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 1 (B)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 2
Bila persen hasil reaksi:
3 NO2(g) + H2O(l) → 2 HNO3(aq) + NO(g)
adalah 75,0%, dan dalam reaksi tersebut dikonsumsi sebanyak 45,0 g gas NO2, berapa gram gram asam nitrat, HNO3 (aq), yang dihasilkan?
A. 22,5 g
B. 30,8 g
C. 41,1 g
D. 54.8 g
E. 69,3 g
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 2
45 g NO₂ = 45g : 46 g/mol = 0,978 mol
3NO2 + H2O ⟶ 2HNO3 + NO
Mol HNO3= 2/3 x 0,978 mol = 0,652 mol
Hasil reaksi 75% maka HNO₃ yang dihasilkan = 75% × 0,6522 mol = 0,48915 mol
Massa HNO3 = 0,48915 mol × Mr HNO3
Massa HNO₃ = 0,48915 mol × 63 g/mol
Massa HNO₃ = 30,8 gram
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 2 (B)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 3
Suatu pil sakit kepala mengandung 200 mg ibuprofen (C13H18O2; 206 g/mol) diminum dengan 0,5 L air oleh siswa yang perutnya kosong. Bila semua pil tersebut larut, berapakah molalitas larutan yang terbentuk dalam perut siswa tersebut?
A. 2,3 x 10-3 m
B. 4,1 x 10-3 m
C. 9,7 x 10-4 m
D. 1,9 x 10-3 m
E. 1,7 x 10-2 m
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 3
Molalitas = mol zat terlarut : massa pelarut
Massa molar C13H18O2 = 13×12 + 18×1 + 2×16 = 206 g/mol
0,2 g C13H18O2 = 0,2 g : 206 g/mol = 0,00097 mol
Molalitas larutan = 0,00097 mol: 0,5 kg (asumsi massa jenis air 1 g/mL)
Molalitas larutan = 0,00194 = 1,9 × 10–3 molal
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 3 (D)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 4
Pada tekanan 50 kPa dan 127 oC, sebanyak 100 cm3 gas pada memiliki massa 0,120 g. Berapa massa molekular relatif gas ini?
A. 1,2
B. 25
C. 80
D. 120
E. 160
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 4
1 atm = 101325 Pa ⟶ 50.000 Pa = 0,49346 atm
PV = nRT
0,49346 atm × 0,1 L = n × 0,082 L.atm.mol-1.K-1 × 400 K
0,049346 atm.L = n × 32,82 L.atm.mol-1
n = 0,001504 mol
Massa molar = 0,12 g / 0,001504 mol = 79,81 g/mol
Jawaban yang paling mendekati yakni 80 g/mol
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 4 (C)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 5
Susunlah bagaimana urutan kelarutan zat berikut ini didalam air:
KCl, CH3CH2COOH, CH3CH2CH3, CH3CH2CH2OH, dan CH3C-O-CH3
A. KCl < CH3CH2COOH < CH3CH2CH3 < CH3CH2CH2OH < CH3C-O-CH3
B. KCl < CH3CH2CH2OH < CH3CH2CH3 < CH3CH2COOH < CH3C-O-CH3
C. CH3CH2CH3 < KCl < CH3C-O-CH3 < CH3CH2CH2OH < CH3CH2COOH
D. CH3CH2COOH < CH3CH2CH2OH < CH3C-O-CH3 < CH3CH2CH3 < KCl
E. CH3CH2CH3 < CH3C-O-CH3 < CH3CH2CH2OH < CH3CH2COOH < KCl
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 5
Zat yang gampang larut dalam air yakni senyawa ion berikutnya yakni senyawa polar dan yang sulit larut dalam air yakni senyawa nonpolar.
Jadi urutannya yakni CH3CH2CH3 < CH3C(O)CH3 < CH3CH2CH2OH < CH3CH2COOH < KCl
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 5 (E)
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 1 – 10
Download PDF DOC | Soal OSP Kimia 2015 Nomor 6
Suatu zat padat padat memiliki titik leleh yang tajam dan terang di atas 100°C. Zat padat tersebut tidak sanggup menghantar listrik bahkan dalam keadaan lelehan, dan larut dalam pelarut hidrokarbon. Apakah struktur yang paling seolah-olah mengenai zat padat tersebut?
A. Kristal atomik
B. Kristal ionik
C. Kristal molekular raksasa
D. Kristal molekular
E. Logam.
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 6
Pada soal ini bahu-membahu sedikit agak mencurigai untuk menjawab D alasannya yakni tidak berlaku mutlak untuk semua sifat yang disebutkan. Oleh lantaran itu di sini hanya ditinjau yang memang mungkin dan mustahil saja.
- Kristal atomik → titik leleh relatif rendah
- Kristal ionik → sukar larut dalam pelarut hidrokarbon, titik leleh sangat tinggi
- Kristal molekular raksasa → sulit larut dalam pelarut organik.
- Kristal molekular → titik leleh moderat (tidak terlalu rendah/tinggi), tidak sanggup menghantar arus listrik, sebagian larut dalam
- Logam → menghantarkan arus listrik
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 6 (D)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 7
Suatu sampel dari senyawa X, kalau dipanaskan dengan larutan natrium hidroksida akan menghasilkan gas A. Bila X dipanaskan dengan asam sulfat pekat, akan dihasilkan gas B. Bila gas A dan B direaksikan, maka akan dihasilkan kembali senyawa X. Berikut ini, manakah yang merupakan senyawa X?
A. CH3CO2C2H5
B. NH2CH2CO2CH3
C. NH4Cl
D. NH4I
E. (NH4)2SO4.
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 7
Dari pilihan yang tersedia yang paling mungkin yakni NH4Cl dengan kemungkinan reaksi:
NH4Cl(aq) + NaOH(aq) → NaCl(aq) + NH3 (g)+ H2O(l)
2NH4Cl(aq) + H2SO4 (aq)→ (NH4)2SO4(aq) + 2HCl(g)
NH3 (g)+ HCl(g) → NH4Cl
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 7 (C)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 8
Pernyataan manakah yang sanggup menjelaskan bahwa endapan magnesium hidroksida sanggup larut dalam larutan aqua NH4Cl, tetapi tidak larut dalam larutan aqua NaCl?
A. Dalam air, larutan NH4Cl menghasilkan NH4OH, dan ion OH– yang terbentuk kemudian memperlihatkan efek ion sejenis.
B. Ion NH4+ dalam larutan NH4Cl akan menurunkan nilai hasil kali kelarutan Mg(OH)2.
C. Larutan garam NH4Cl kurang berdisosiasi tepat dibandingkan larutan NaCl.
D. Ion Na+ dan ion Mg2+ adalah isoelektronik (mempunyai jumlah elektron sama).
E. Ion NH4+ dalam air akan menghasilkan sejumlah H3O+
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 8
Peristiwa ini terkait dengan garam yang sanggup bereaksi dengan air (mengalami hidrolisis). NH4Cl dalam air akan terurai menjadi NH4+ dan Cl–, Cl– tidak sanggup terhidrolisis sedang NH4+terhidrolisis sesuai reaksi :
NH4+ + 2H2O → NH4OH + H3O+ . Ion H3O+
inilah yang kemudian sanggup bereaksi dengan OH– yang berasal dari Mg(OH)2 sehingga Mg(OH)2 dikatakan sanggup larut dalam larutan NH4Cl.
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 8 (E)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 9
Alanine, H2NCH(CH3)CO2H, yakni suatu asam amino dengan nilai Ka = 4,5 × 10–3 dan Kb =7,4 × 10–5. Di dalam air, spesi manakah yang memiliki konsentrasi paling tinggi pada pH 7?
A. H2NCH(CH3)CO2H
B. +H3NCH(CH3)CO2H
C. H2NCH(CH3)CO–
D. +H3NCH(CH3)CO2–
E. Semua jawaban, A, B, C dan D benar
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 9
H2NCH(CH3)CO2H ini sanggup bersifat sebagai asam dan sekaligus sanggup bersifat sebagai basa. 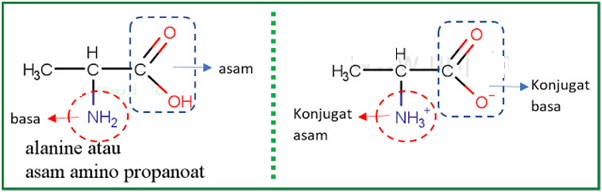
pKa = -log(4,5 × 10–3) = 2,35
pKb = -log(7,4 × 10–5) = 4,13
pH = 7 → pOH = 7
Untuk menjawab ini sanggup dipakai persamaan Henderson-Hasselbalch:
pH = pKa + log([konjugat basa][asam])
7 = 2,35 + log([konjugat basa][asam])
agar sanggup memenuhi syarat pH = 7, [konjugat basa] harus lebih besar dari [asam] dengan kata lain spesi CO2– harus punya konsentrasi lebih tinggi.
pOH = pKb + log([konjugat asam][basa])
7 = 4,13 + log ([konjugat asam][basa])
agar sanggup memenuhi syarat pOH = 7, [konjugat asam] harus lebih besar dari [basa] dengan kata lain spesi NH3+ harus punya konsentrasi lebih tinggi.
Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 9 (D)
Download PDF DOC | Soal OSP Kimia 2015 Nomor 10
Pada molekul berikut ini,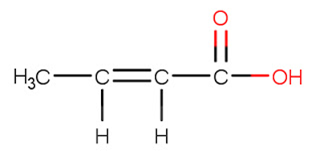
ada berapa banyak atom karbon yang memiliki hibridisasi sp2
A. 0
B. 1
C. 2
D. 3
E. 4
Download PDF DOC | Pembahasan Soal Kimia OSP 2015 Nomor 10
Atom C memiliki ikatan tunggal saja hibridisasinya yakni sp3
Atom C memiliki 1 ikatan dobel hibridisasinya yakni sp2
Atom C memiliki 1 ikatan tripel atau 2 ikatan dobel hibridisasinya yakni sp

Download PDF DOC | Kunci Jawaban Soal Kimia OSP 2015 Nomor 10 (D
Demikian tadi pembahasan soal Kimia OSP 2015 untuk nomor 1 sampai 10. Untuk nomor selanjutnya sanggup di saluran melalui link di bawah ini.
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 1 – 10
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 11 – 20
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 21 – 30
Pembahasan Soal OSN Provinsi (OSP) Kimia 2015 Nomor 1 – 10
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon