Download dan Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 21 – 30 – Soal UN berbasis kertas telah dirilis oleh sahabat dan sanggup di d0wnl0ad di internet. Ini sangat bermanfaat untuk murid-murid yang akan melakukan UN 2019 tahun depan mata pelajaran Kimia. Postingan ini melanjutkan goresan pena sebelumnya, yakni Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 21 – 30. Untuk nomor 1 sampai 20 sanggup dilihat di postingan sebelumnya.
Download dan Pembahasan Soal
SOAL UNBK Kimia Tahun 2018 Nomer 21 – 25
Soal UNBK Kimia 2018 Nomer 21
Jika monomer asam adipat (asam-heksanadioat) dan monomer heksametilendiamina (1,6-diamino heksana) membentuk polimer secara kondensasi, polimer yang dihasilkan yaitu ….
- nilon 6,6
- PVC
- teflon
- terilen
- bakelit
Pembahasan Soal UNBK Kimia 2018 Nomer 21
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 21 : A
Ini merupakan soal hafalan
Nilon 6,6 : asam adipat dan heksametilendiamina
Teflon : tetrafluorotena
PVC : vinil klorida
Terilen : suatu dialkohol dan suatu dikarbosilat
Bakelit : fenol dan formaldehid
Soal UNBK Kimia 2018 Nomer 22
Perhatikan gambar lintasan elektron ion M2+ dan L– berikut!
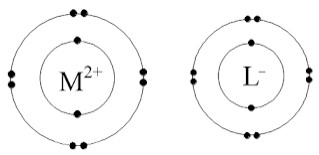
Unsur M dan L masing-masing mempunyai jumlah neutron berturut-turut 12 dan 10. Berdasarkan data tersebut, pernyataan yang sempurna yaitu …
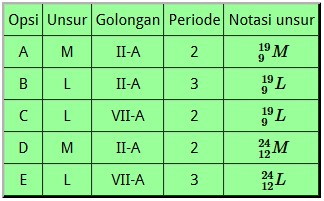
Pembahasan Soal UNBK Kimia 2018 Nomer 22
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 22 : C
Ingat :
ION POSITIF –> ATOM = elektron ditambah (menjadi nomor atom)
ION NEGATIF –> ATOM = elektron dikurangi (menjadi nomor atom)
M2+ mempunyai 10 elektron, maka atom M mempunyai nomor 12
Konfigurasi elektron M = 2-8-2
→ golongan II-A, periode-3
Nomor atom M = 12
Nomor massa M = jumlah netron M + nomor atom M
Nomor massa M = 12 + 12 = 24
L– mempunyai 10 elektron, maka atom L mempunyai nomor 9
Konfigurasi elektron L = 2-7
→ golongan VII-A, periode-2
Nomor atom L = 9
Nomor massa L = jumlah netron L + nomor atom L
Nomor massa L = 10 + 9 = 19
Soal UNBK Kimia 2018 Nomer 23
Seorang siswa ingin memilih orde reaksi dari reaksi antara natrium tiosulfat dan asam klorida menghasilkan natrium klorida, air dan welirang dioksida dan endapan welirang berdasarkan reaksi:
Na2S2O3(aq) + 2HCl(aq) → 2NaCl(aq) + H2O(l) + SO2(g) + S(s)
Percobaan dilakukan dengan mengukur kecepatan terbentuknya endapan belerang. Data hasil percobaan disajikan pada tabel berikut ini.
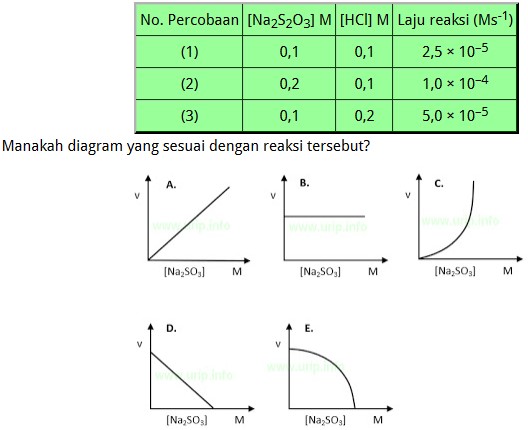
Pembahasan Soal UNBK Kimia 2018 Nomer 23
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 23 : C
Untuk memilih orde Na2SO3 kita memakai data nomor 2 dan 1 sebab konsentrasi HCl tetap.
([Na2SO3]2/[ Na2SO3]1)x = v2/v1
(0,2/0,1)x = 1×10–4 / 2,5×10–5
2x = 4
2x = 22
x = 2
Grafik laju reaksi orde 2 yang benar yaitu C
Soal UNBK Kimia 2018 Nomer 24
Respirasi aerob yaitu kejadian pemecahan glukosa dengan sumbangan oksigen menghasilkan energi dalam bentuk ATP. Persamaan reaksi untuk pemecahan satu molekul glukosa secara sederhana yaitu sebagai berikut.
C6H12O6(aq) + O2 (g) → CO2(g) + H2O(g) (belum setara)
Pada respirasi aerob terjadi pembakaran 5,4 g glukosa (Ar C = 12, H = 1, O = 16) dan gas oksigen yang tersedia yaitu 6,4 g. Gas karbon dioksida yang dihasilkan pada kejadian tersebut kalau diukur pada keadaan STP yaitu …
- 4,480 L
- 4,032 L
- 3,584 L
- 2,688 L
- 0,672 L
Pembahasan Soal UNBK Kimia 2018 Nomer 24
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 24 : A
Volume gas-gas dalam reaksi akan sebanding dengan koefisien reaksi gas dalam persamaan reaksi yang setara. Pada keadaan STP setiap 1 mol gas = 22,4 L
Reaksi setara: C6H12O6(aq) + 6O2 (g) → 6CO2(g) + 6H2O(g)
Massa molar C6H12O6 = ((12×6)+(1×12)+(16×6)) g/mol = 180 g/mol
5,4 g C6H12O6 = 5,4 g : 180 g/mol = 0,03 mol
Massa molar O2 = 16×2 = 32 g/mol
6,4 g O2 = 6,4 g : 32 g/mol = 0,2 mol
Penentuan pereaksi pembatas, zat mana yang habis bereaksi yang akan digunkan sebagai pembanding untuk memilih jumlah mol CO2.
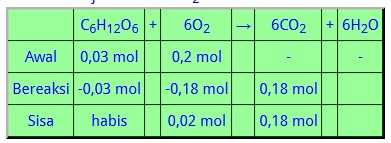
Jadi volume CO2 = 0,18 mol × 22,4 L/mol = 4,032 L
Soal UNBK Kimia 2018 Nomer 25
Tabel larutan penyangga beserta komposisinya.
| No. | Larutan Asam | Larutan Garam |
| (1) | 10 mL larutan HF 0,02 M | 10 mL larutan NaF 0,01 M |
| (2) | 10 mL larutan HF 0,04 M | 10 mL larutan KF 0,01 M |
| (3) | 10 mL larutan HF 0,06 M | 10 mL larutan NaF 0,01 M |
Diketahui Ka HF = 6,8×10–4 urutan harga pH mulai dari yang terkecil sampai ke terbesar yaitu ….
- (1), (2), (3)
- (1), (3), (2)
- (2), (1), (3)
- (2), (3), (1)
- (3), (2), (1)
Pembahasan Soal UNBK Kimia 2018 Nomer 25
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 25 : E
[H+] = Ka[asam lemah]/[basa konjugat]
Karena konsentrasi basa konjugat tetap, maka [H+] hanya ditentukan [asam lemah]. Semakin besar [asam lemah] maka [H+] semakin tinggi. pH = – log [H+], pH ini berbanding terbalik dengan [H+], semakin besar [H+] maka pH semakin kecil.
Jadi urutan yang benar yaitu (3), (2), (1)
Download dan Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 26 – 30
Soal UNBK Kimia 2018 Nomer 26
Diketahui 2 buah rumus struktur senyawa turunan alkana berikut ini.

Perbedaan sifat kimia dari kedua senyawa tersebut yaitu ….
- senyawa X sanggup bereaksi dengan Fehling membentuk cermin perak sedangkan senyawa Y tidak sanggup bereaksi
- senyawa X sanggup bereaksi dengan logam natrium sedangkan senyawa Y tidak sanggup bereaksi
- senyawa Y sanggup membentuk ikatan hidrogen sedangkan senyawa X tidak dapat
- senyawa X sanggup bereaksi dengan HCN sedangkan senyawa Y tidak sanggup bereaksi dengan HCN
- senyawa Y mempunyai titik didih lebih rendah dibanding senyawa X dengan Mr yang sama
Pembahasan Soal UNBK Kimia 2018 Nomer 26
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 26 : B
Materi hafalan
Senyawa X : alkohol
Senyawa Y : eter
Uji Fehling untuk menguji keberadaan gugus aldehid
X memang sanggup bereaksi dengan Na sedangkan Y tidak sanggup bereaksi dengan Na
Y tidak sanggup membentuk ikatan hidrogen dan X dapat
Dengan Mr yang sama X akan mempunyai titik didih lebih tinggi sebab adanya ikatan hidrogen
Soal UNBK Kimia 2018 Nomer 27
Massa garam dapur yang harus ditaburkan ke dalam 1 ton salju semoga titik beku air salju turun menjadi -5oC yaitu … (Ar Na = 23, Cl = 35,5, Kf air = 1,86 molal –1 .oC)
- 39,310 kg
- 78,629 kg
- 393,100 kg
- 786,290 kg
- 78629 kg
Pembahasan Soal UNBK Kimia 2018 Nomer 27
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 27 : B
NaCl akan terurai menjadi 2 partikel (Na+ dan Cl–), faktor van Hoff (i) = 2
∆Tb = 0 – (–5) = 5
massa air = 1 ton = 1.000 kg
Massa molar NaCl = (23+35,5) g/mol = 58,5 g/mol
∆Tb = molalitas NaCl × Kf × i
5 = molalitas NaCl × 1,86 × 2
molalitas NaCl = (5 : 3,72) molal
molalitas NaCl = 1,344 molal
Molalitas = jumlah mol zat terlarut : massa pelarut (kg)
1,344 molal = jumlah mol NaCl : 1.000 kg
Jumlah mol NaCl = 1,344 molal ×1.000 kg
Jumlah mol NaCl = 1.344 mol
Massa NaCl = jumlah mol NaCl × massa molar NaCl
Massa NaCl = 1.344 mol × 58,5 g/mol
Massa NaCl = 78.624 g = 78,624 kg.
Soal UNBK Kimia 2018 Nomer 28
iketahui harga Ksp CaSO4 = 7,1 × 10–5
Larutan yang tertera pada tabel di bawah ini dicampurkan.
| No. | 100 mL larutan | 100 mL larutan |
| (1) | Ca(OH)2 6 × 10–5 M | Na2SO4 6 × 10–5 M |
| (2) | CaCl2 6 × 10–5 M | Na2SO4 6 × 10–5 M |
| (3) | CaCl2 5 × 10–2 M | Na2SO4 5 × 10–2 M |
| (4) | Ca(NO3)2 5 × 10–4 M | Na2SO4 5 × 10–4 M |
| (5) | Ca(NO3)2 5 × 10–2 M | K2SO4 5 × 10–1 M |
Campuran yang menghasilkan endapan yaitu ….
- (1) dan (2) sebab nilai Qc > Ksp
- (1) dan (4) sebab nilai Qc > Ksp
- (2) dan (5) sebab nilai Qc = Ksp
- (3) dan (5) sebab nilai Qc > Ksp
- (4) dan (5) sebab nilai Qc < Ksp
Pembahasan Soal UNBK Kimia 2018 Nomer 28
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 28 : DSyarat terbentuknya endapan nilai Qc > Ksp
Qc yang nilainya lebih besar dari Ksp CaSO4 :
(3) Qc = (5×10–2)(5×10–2) = 2,5×10–3
(4) Qc = (5×10–2)(5×10–1) = 2,5×10–2
Soal UNBK Kimia 2018 Nomer 29
Biosolar merupakan adonan biodisel dan solar. Biodiesel dibentuk melalui reaksi transesterifikasi minyak/lemak dengan alkohol dan basa berpengaruh menghasilkan monoalkilester dan gliserin sebagai hasil samping. Sedangkan solar sanggup diperoleh dari pengolahan minyak bumi yang kandungannya terdiri atas senyawa-senyawa alkana rantai panjang C16–C20.
Berdasarkan wacana tersebut, struktur senyawa komponen utama biodiesel dan solar yaitu …

Pembahasan Soal UNBK Kimia 2018 Nomer 29
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 29 : B
Sudah jelas
Soal UNBK Kimia 2018 Nomer 30
Pembuatan amonia (bahan dasar pupuk) diproduksi secara besar-besaran melalui proses Haber-Bosch berdasarkan persamaan kesetimbangan:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Reaksi tersebut memakai katalis.
Hubungan efek suhu terhadap nilai konstanta kesetimbangan pada proses tersebut, diberikan pada tabel berikut.
| Suhu (oC) | Kp (atm-2) |
| 500 | 0,4 |
| 400 | 0,7 |
Berdasarkan data, pernyataan yang benar wacana kesetimbangan pembentukan amonia yaitu ….
- endoterm, suhu dinaikkan kesetimbangan bergeser ke arah pembentukan amonia (kanan)
- endoterm, suhu dinaikkan kesetimbangan bergeser ke arah pembentukan N2 dan H2 (kiri)
- eksoterm, suhu diturunkan kesetimbangan bergeser ke arah pembentukan N2 dan H2 (kiri)
- eksoterm, suhu diturunkan kesetimbangan bergeser ke arah pembentukan amonia (kanan)
- endoterm, peningkatan suhu hanya mempercepat tercapainya kesetimbangan baru
Pembahasan Soal UNBK Kimia 2018 Nomer 30
Kunci Jawaban Soal Kimia UNBK 2018 Nomer 30 : D
Pada reaksi yang bersifat endoterm (membutuhkan kalor) ke arah kanan pada sistem kesetimbangan reaksi akan semakin menghasilkan produk di ruas kanan bila temperatur dinaikkan. Sebaliknya pada reaksi yang bersifat eksoterm (menghasilkan kalor) ke arah kanan pada sistem kesetimbangan reaksi malah akan mengurangi produk di ruas kanan bila temperatur dinaikkan.
Dari tabel diketahui nilai Kp yang semakin besar berarti produk bertambah konsentrasinya. Ini mengindikasikan reaksi bergeser ke kanan (ke arah pembentukan NH3).
Karena reaksi bergeser ke kanan dikala suhu di turunkan dari 500 oC menjadi 400 oC bermakna reaksi tersebut bersifat eksoterm.
Demikian tadi pembahasan soal UN Kimia 2018 nomor 21 – 30, untuk nomor lain, silahkan baca di bawah ini. Semoga bermanfaat.
Thanks to pak urip.info atas ketikan dan pembahasannya
Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 1 – 10
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 11 – 20
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 21 – 30
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 31 – 40
Download dan Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 21 – 30
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon