Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 1 – 10 – Alhamdulillah, jadinya pak Urip.info merilis Pembahasan Soal UNBK 2018 untuk mapel Kimia. Untuk murid-murid, ini sanggup dipakai untuk persiapan UNBK 2019 mendatang. Pesan beliau, jikalau dalam Pembahasan Soal terdapat kesalahan, mohon dikoreksi. Berikut ini soal dan kunci balasan UNBK Kimia tahun 2018.
Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 1 – 10
Soal Nomer 1 | UNBK KIMIA
Cermati ihwal berikut!
Apabila kita ingin memberantas lintah atau pacet yang berkeliaran di sekitar rumah daerah tinggal, kantor daerah bekerja, sekolah dan daerah lainnya, kita sanggup memanfaatkan garam dapur. Garam dapur ditaburkan di tempat-tempat yang sering dilewati lintah atau pacet. Lintah sangat sensitif dengan garam. Jika kulitnya terkena garam dalam jangka waktu yang cukup lama, maka lintah sanggup mati.
Penggunaan garam dapur untuk membasmi lintah menyerupai pada ihwal tersebut merupakan pemanfaatan sifat koligatif larutan, yaitu tekanan osmotik alasannya partikel garam dapur menyebabkan….
A. suhu badan lintah naik
B. suhu badan lintah turun
C. tekanan darah lintah naik
D. tekanan darah lintah turun
E. cairan dalam badan lintah keluar
Pembahasan soal nomer 1 | UNBK KIMIA
Kunci balasan : E
Cairan dalam badan lintah akan keluar melalui membran membentuk larutan garam alasannya kejadian berpindahnya pelarut dari larutan lebih encer melalui selaput membran/pori ke larutan berkonsentrasi lebih tinggi
Soal Nomer 2 | UNBK KIMIA
Diketahui energi ikatan rata-rata sebagai berikut.
N≡N = 914 kJ/mol
H−H = 436 kJ/mol
N−H = 391 kJ/mol
Pada penguraian 4,25 gram amonia menjadi gas hidrogen dan gas nitrogen akan membutuhkan jumlah kalor sebanyak… (Ar N = 14, H = 1)
A. 248 kJ
B. 124 kJ
C. 62 kJ
D. 31 kj
E. 15,5 kj
Pembahasan soal nomer 2 | UNBK KIMIA
Kunci Jawaban E
Reaksi setara penguraian amonia:
2NH3 → N2 + 3H2
∆H untuk penguraian 2 mol NH3
2(3[N−H]) → N≡N + 3(H−H)
∆H = Total energi pemutusan ikatan di ruas kiri – Total energi pembentukan ikatan di ruas kanan
∆H = 2(3×391 kJ/mol) – (914 kJ/mol + 3(436 kJ/mol))
∆H = 2.346 kJ – 2.222 kJ
∆H = 124 kJ
→ ∆H permol = 124 kJ : 2 mol = 62 kJ/mol
Penguraian 4,25 gram NH3 :
Massa molar NH3 = 14 + 3(1) = 17 gram/mol
Jumlah mol NH3 = 4,25 gram : 17 gram/mol
Jumlah mol NH3 = 0,25 mol
Jadi ∆H untuk 0,25 mol NH3 = 62 kJ/mol × 0,25 mol
Jadi ∆H untuk 0,25 mol NH3 = 15,5 kJ
Soal Nomer 3 | UNBK KIMIA
Perhatikan trayek pH dan indikator berikut!
| Indikator | Trayek pH |
| Methyl orange | 3,1 – 4,4 |
| Phenolftalein | 8,0 – 9,8 |
| Bromthymol Blue | 6,0 – 7,6 |
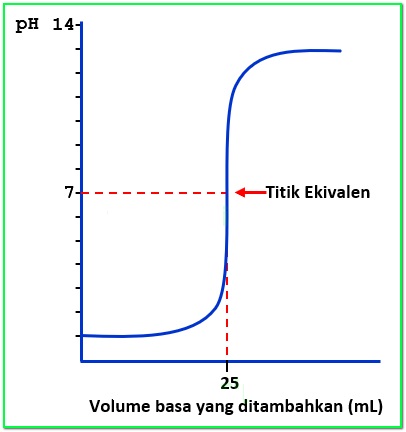
Berdasarkan grafik tersebut, pasangan larutan asam-basa dan indikator yang dipakai pada titrasi tersebut yaitu …
A. larutan CH3COOH dititrasi oleh larutan NaOH dengan indikator bromthymol blue
B. larutan CH3COOH dititrasi oleh larutan NH4OH dengan indikator phenolftalein
C. larutan CH3COOH dititrasi oleh larutan NaOH dengan indikator methyl orange
D. larutan HCl dititrasi oleh larutan NaOH dengan indikator phenolftalein
E. larutan HCl dititrasi oleh larutan NH4OH dengan indikator phenolftalein
Pembahasan soal nomor 3 | UNBK KIMIA
Kunci Jawaban : D
Dari gambar menawarkan titik ekuivalen = 7, artinya pasangan larutan berasal dari asam besar lengan berkuasa dan basa kuat.
Soal Nomer 4 | UNBK KIMIA
Diketahui data tabel berikut.
| No | Kation Logam | Anion Nonlogam | Rumus Kimia | Nama Senyawa |
| (1) | B3+ | Cl– | BCl3 | Boron triklorida |
| (2) | Fe2+ | O2– | FeO | Besi oksida |
| (3) | Pb2+ | S2– | PbS2 | Timbal (IV) sulfida |
| (4) | Al3+ | S2– | Al2S3 | Aluminium sulfida |
Berdasarkan tabel data tersebut, pasangan data yang benar pada tabel tersebut terdapat pada nomor…
A. (1) dan (2)
B. (1) dan (3)
C. (2) dan (3)
D. (2) dan (4)
E. (3) dan (4)
Pembahasan soal nomer 4 | UNBK KIMIA
Kunci Jawaban : 1 dan 4
Berikut ini yaitu data yang seharusnya:
| No | Kation Logam | Anion Nonlogam | Rumus Kimia | Nama Senyawa |
| (1) | B3+ | Cl– | BCl3 | Boron triklorida |
| (2) | Fe2+ | O2– | FeO | Besi (II) oksida |
| (3) | Pb2+ | S2– | PbS2 | Timbal (II) sulfida |
| (4) | Al3+ | S2– | Al2S3 | Aluminium sulfida |
Soal Nomer 5 | UNBK KIMIA
Tes gula darah dalam urin sanggup dilakukan dengan memakai reaksi reduksi yaitu dengan memakai pereaksi….
A. Fehling, alasannya menguji adanya gugus aldehid dalam gula
B. Biuret, alasannya menguji adanya ikatan peptida
C. Benedict, alasannya menguji adanya gugus keton dalam gula
D. Lugol, alasannya menguji adanya gugus benzena dalam senyawa
E. Millon, alasannya menguji adanya gugus sulfur dalam darah
Pembahasan Soal Nomer 5 | UNBK KIMIA
Kunci Jawaban : C
Uji Fehling bertujuan untuk mengetahui adanya gugus aldehid dalam gula
Uji Benedict bertujuan untuk mengetahui kandungan gula (karbohidrat) pereduksi
Uji Biuret bertujuan untuk mengetahui ikatan peptida
Lugol bertujuan untuk uji ada tidaknya amilum
Millon bertujuan untuk mengetahui adanya asam tirosin
Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 1 – 10
Soal Nomer 6 | UNBK KIMIA
Jika unsur A (nomor atom 7) dan B (nomor atom 17) berikatan, struktur lewis yang benar adalah…

Pembahasan Soal Nomer 6 | UNBK KIMIA
Kunci Jawaban : C
Struktur Lewis yaitu simbol atom dikelilingi jumlah elektron valensi
Unsur A bervalensi 5 (sebagai atom pusat) : membutuhkan 3 elektron untuk mencapai oktet
Unsur B bervalensi 7 : membutuhkan 1 elektron untuk mencapai oktet
A dan B saling meminjamkan elektron, alasannya unsur B hanya sanggup meminjamkan 1 elektron padahal unsur A membutuhkan 3 elektron, maka dimunculkan unsur B sebanyak 3, sehingga membentuk menyerupai gambar C dengan atom pusat mempunyai 1 pasangan elektron bebas (PEB)
Soal nomer 7 | UNBK KIMIA
Diketahui 3 data entalpi pembentukan senyawa
∆Hof CH3OH(g) = –725 kJ/mol
∆Hof CO2(g) = –394 kJ/mol
∆Hof H2O (g) = –242 kJ/mol
Entalpi pembakaran standar metanol berdasarkan reaksi:
CH3OH(g) + 1½ O2(g) → CO2(g) + 2H2O(g) yaitu …
A. –1257 kJ/mol
B. –1105 kJ/mol
C. –153 kJ/mol
D. +153 kJ/mol
E. +1257 kJ/mol
Pembahasan soal nomer 7 | UNBK KIMIA
Kunci balasan : C
Pembakaran standar yaitu pembakaran 1 mol zat yang dilakukan pada keadaan standar.
∆Hco = S∆Hfo (produk) – S∆Hfo (pereaksi)
∆Hco CH3OH = (∆Hfo CO2 + 2.∆Hfo H2O ) – ∆Hfo CH3OH
∆Hco CH3OH = (–394 + 2.( –242)) – (–725 kJ)
∆Hco CH3OH = –878 kJ + 725 kJ
∆Hco CH3OH = –153 kJ
Soal Nomer 8
Data dari suatu unsur sebagai berikut.
- Digunakan dalam industri pesawat terbang
- Senyawa sulfatnya dipakai sebagai komponen dalam tawas
- Dapat bereaksi dengan NaOH
- Termasuk unsur tahan korosi
Unsur yang mempunyai sifat tersebut yaitu unsur….
A. Fe
B. Mg
C. Sn
D. Cu
E. Al
Pembahasan soal Nomer 8 | UNBK KIMIA
Kunci Jawaban : E
Badan pesawat terbuat dari aluminium alasannya ringan
Tawas K2SO4.Al2(SO4)3.24H2O.
Reaksi Al dengan NaOH: 2Al + 2NaOH → 2NaAlO2 + H2↑
Al tahan karat maka banyak dipakai untuk perabot dapur
Soal Nomer 9 | UNBK KIMIA
Perhatikan data hasil uji daya hantar listrik terhadap beberapa larutan di bawah ini!
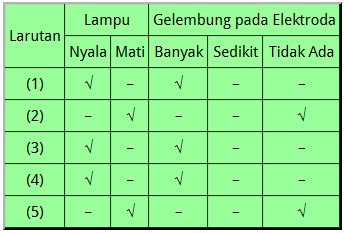 Berdasarkan data tersebut, pasangan larutan yang mempunyai derajat ionisasi sama dengan nol yaitu ….
Berdasarkan data tersebut, pasangan larutan yang mempunyai derajat ionisasi sama dengan nol yaitu ….
A. (1) dan (2)
B. (1) dan (4)
C. (2) dan (3)
D. (2) dan (5)
E. (3) dan (5)
Pembahasan soal Nomer 9 | UNBK KIMIA
Kunci Jawaban : D
Derajat ionisasi sama dengan nol artinya larutan tersebut termasuk larutan nonelektrolit
Ditandai dengan lampu mati dan tidak adanya gelembung gas
Soal Nomor 10 | UNBK KIMIA
Perhatikan tabel berikut!

Pasangan data yang sempurna terdapat pada larutan garam nomor…
A. (1) dan (2)
B. (1) dan (4)
C. (2) dan (3)
D. (2) dan (4)
E. (3) dan (4)
Pembahasan soal Nomer 10 | UNBK KIMIA
Kunci Jawaban : D

Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 1 – 10
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 11 – 20
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 21 – 30
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 31 – 40
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 1 – 10
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon