Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 11-20 – Dalam mempersiapkan seleksi Olimpiade Sains Nasional tingkat Provinsi (OSP) tahun 2019, perlu adanya pembahasan soal OSP 2018. Untuk mapel Kimia, berikut ini yaitu pembahasan soal OSP Kimia tahun 2018 PDF klik logo print.Ke depan saya sediakan Pembahasan Soal OSP Kimia 2019.
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 11-20
Soal OSP Kimia 2018 Nomer 11
Pada masing-masing reaksi kesetimbangan dalam pilihan balasan di bawah ini dilakukan dua perubahan yang terpisah:
(i) tekanan diturunkan pada suhu tetap;
(ii) suhu dinaikkan pada tekanan tetap.
Di antara reaksi kesetimbangan berikut, manakah yang menghasilkan kenaikan dalam jumlah produk ketika kedua perubahan di atas dilakukan adalah:
A. H2(g) + l2(g) ⇌ 2Hl(g) ;
B. 4NH3(g) + 5O2(g) ⇌ 4NO(g) + 6H2O(g);
C. N2(g) + 3H2(g) ⇌ 2NH3(g);
D. N2O4(g) ⇌ 2NO2(g);
E. CO(g) + H2O(g) ⇌ CO2(g) + H2(g);
Pembahasan Soal OSP Kimia 2018 Nomer 11
Dalam sistem kesetimbangan berlaku:
(i) tekanan diturunkan pada suhu tetap.
Jika tekanan diturunkan pada suhu tetap maka kesetimbangan akan bergeser ke arah jumlah zat (koefisien zat) terbesar.
Analisis:
Reaksi A, jumlah zat reaktan (2) = jumlah zat produk (2), tidak terjadi pergeseran
Reaksi B, jumlah zat reaktan (9) < jumlah zat produk (10), jumlah produk naik
Reaksi C, jumlah zat reaktan (4) > jumlah zat produk (2), jumlah produk turun
Reaksi D, jumlah zat reaktan (1) < jumlah zat produk (2), jumlah produk naik
Reaksi E, jumlah zat reaktan = jumlah zat produk, tidak terjadi pergeseran
(ii) suhu dinaikkan pada tekanan tetap
Jika suhu dinaikkan, kesetimbangan akan bergeser ke arah reaksi yang bersifat endoterm
Analisis:
Reaksi A ke kanan bersifat endoterm, jumlah produk naik
Reaksi B ke kanan bersifat eksoterm, jumlah produk turun
Reaksi C ke kanan bersifat eksoterm, jumlah produk turun
Reaksi D ke kanan bersifat endoterm, jumlah produk naik
Reaksi E ke kanan bersifat eksoterm, jumlah produk turun
Dari kedua perubahan, reaksi yang sanggup mengalami kenaikan jumlah produk yaitu reaksi D.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 11 yang sempurna D
Soal OSP Kimia 2018 Nomer 12
Perhatikan reaksi kesetimbangan berikut:
CH3COOH(aq) ⇌ CH3COO–(aq) + H+(aq) + kalor
Pada dikala t1, sistem kesetimbangan mengalami gangguan menyerupai plot pada grafik berikut:

Gangguan yang diberikan pada dikala t1 yaitu sebagai akhir dari:
A. Penambahan HCI
B. Suhu diturunkan
C. Penambahan NaCH,COO
D. Penambahan CH,COOH
E. Volume wadah bertambah
Pembahasan Soal OSP Kimia 2018 Nomer 12
CH3COOH(aq) ⇌ CH3COO–(aq) + H+(aq) + kalor
Pada kurva/grafik tampak bahwa [H+] turun dikala t1. Ini berarti reaksi bergeser ke kiri, ke arah reaktan.
Analisis:
- Penambahan HCl berarti menambah [H+] yang ada di sisi produk reaksi memang akan meningkatkan jumlah reaktan, tetapi [H+] ini secara keseluruhan sanggup jadi tidak berkurang, alasannya yaitu [H+] yang bereaksi dengan asetat akhir penambahan [H+] dari HCl.
- Reaksi ini bersifat eksoterm, reaksi akan bergeser ke reaktan jikalau suhu dinaikkan dan [H+] akan naik, tidak malah turun.
- Penambahan NaCH3COO, berarti menambah CH3COO– yang akan bereaksi dengan H+sehingga [H+] berkurang.
- Penambahan CH3COOH akan mengakibatkan reaksi bergeser ke arah produk yang berarti akan menaikkan [H+]
- Volume wadah bertambah, maka reaksi akan ke arah produk yang memang mempunyai jumlah zat (lihat koefisien total) yang lebih besar. [H+] juga akan naik.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 12 yang sempurna C
Soal OSP Kimia 2018 Nomer 13
Perbandingan volume yang harus dicampurkan antara larutan NH3 0,1 M (Kb= 2 x 10-5) dan HCI 0,1 M semoga diperoleh larutan buffer yang mempunyai pH = 9 + log 3 adalah:
A. 2:3
B. 3:1
C. 3:5
D. 5:2
E. 5:3
Pembahasan Soal OSP Kimia 2018 Nomer 13
Kunci Jawaban Soal OSP Kimia 2018 Nomer 13 yang tepat
Soal OSP Kimia 2018 Nomer 14
Perhatikan kurva titrasi antara larutan asam lemah dengan larutan natrium hidroksida di bawah ini:

Perkiraan nilai pKa dari asam lemah tersebut adalah:
A. pKa = 2,7
B. pKa 4,5
C. pKa = 7,0
D. pKa = 9,5
E. pKa = 13,0
Pembahasan Soal OSP Kimia 2018 Nomer 14
Titrasi asam lemah dengan basa kuat, pada titik ekuivalen akan terbentuk garam terhidrolisis. Dari grafik tampak bahwa titik ekuivalen terjadi ketika pH = 9,5
pH = ½ (pKw + pKa + log [garam])
2 pH = pKw + pKa + log [garam]
2×9,5 = 14 + pKa + 0
19 = 14 + pKa
pKa = 19 – 14
pKa = 5
Perkiraan pKa yang paling mungkin dan mendekati yaitu 4,5
Kunci Jawaban Soal OSP Kimia 2018 Nomer 14 yang sempurna B
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 11-20
Soal OSP Kimia 2018 Nomer 15
Jika 50,0 ml sampel larutan ammonium hidroksida dititrasi dengan asam sulfat:
2NH4OH(aq) + H2SO4(aq) →(NH4)2SO4(aq) + 2H2O(/)
untuk mencapai titik final dengan indikator metil merah, diharapkan 25,0 ml asam sulfat 0,200 M. Molaritas basa tersebut adalah:
A. 0,100M
B. 0,150M
C. 0,200 M
D. 0,300 M
E. 0,400 M
Pembahasan Soal OSP Kimia 2018 Nomer 15
Berdasarkan persamaan reaksi setara diketahui relasi sebagai berikut.
Jumlah NH4OH = 2 × jumlah H2SO4
50 mL × [NH4OH] = 2(25 mL × 0,2 M)
50 mL × [NH4OH] = 10 mmol
[NH4OH] = 10/50 M = 0,2 M
Kunci Jawaban Soal OSP Kimia 2018 Nomer 15 yang sempurna C
Soal OSP Kimia 2018 Nomer 16
larutan NaCl ditambahkan bertahap ke dalam larutan 0,010 M yang masing-masing mengandung ion Cu+“, Ag+, Au+ dan Tl+. Nilai Ksp masing-masing senyawa kloridanya berturut turut yaitu 1,9×10-1, 1,6×10-10, 2,0×10-13 dan 1,9×10-4. Senyawa klorida yang akan mengendap pertama kali adalah:
A. CuCl(s)
B. AgCl(s)
C. AuCl(s)
D. TICl(s)
E. Semua mengendap pada dikala yang sama
Pembahasan Soal OSP Kimia 2018 Nomer 16
Pada soal diketahui bahwa semua mempunyai larutan sama dan bermuatan sama yaitu +1. Garam yang akan mengendap pertama kali yaitu garam yang mempunyai nilai Ksp yang paling kecil (2×10–13), dalam hal ini AuCl(s)
Kunci Jawaban Soal OSP Kimia 2018 Nomer 16 yang sempurna C
Soal OSP Kimia 2018 Nomer 17
Di antara reaksi berikut ini yang sanggup diungkapkan dengan tetapan kesetimbangan basa, Kb, adalah:
A. [Zn(H2O)6]2+ ⇌ [Zn(H2O)5OH]+ + H+
B. CN– + H+ ⇌ HCN
C. F– + H2O ⇌ HF + OH–
D. Cr3+ + 6H2O ⇌ [Cr(H2O)6]3+
E. AlCl3 + H2O ⇌ Al(OH)3 + 3 HCl
Pembahasan Soal OSP Kimia 2018 Nomer 17
Kb adalah ungkapan untuk tetapan kesetimbangan basa lemah.
Basa lemah jikalau direaksikan dalam air akan menghasilkan OH–.
Reaksi:
F–(aq) + H2O(l) ⇌ HF(aq) + OH–(aq)
F– berperan sebagai basa
Kb = [HF][OH–]/[F–]
Kunci Jawaban Soal OSP Kimia 2018 Nomer 17 yang sempurna C
Soal OSP Kimia 2018 Nomer 18
Suatu sel elektrokimia terdiri dari elektroda perak dan elektroda emas yang masing-masing direndam dalam larutan Ag+ 1 M dan Au+ 1 M. Bila diketahui E0 Ag+IAg = +0,7991 V dan E0 Au+IAu = +1,68 V, maka potensial sel tersebut adalah:
A. -0,44 v
B. 0,00 v
C. +0,44 v
D. +0,88 v
E. +2,48 v
Pembahasan Soal OSP Kimia 2018 Nomer 18
Reaksi yang terjadi:
Ag + Au+ → Ag+ + Au
Jumlah elektron (n) yang terlibat dalam reaksi masing-masing 1 elektron
E0sel = E0 reduksi – E0 oksidasi
E0sel = (1,68 – 0,7991) volt
E0sel = 0,8809 volt
Potensial sel (Esel)
Esel = E0sel – 0,0592/n × log [Ag+]/[Au+]
Esel = 0,8809 – 0,0592/1 × log 1/1
Esel = 0,8809 – 0,0592 × log 1
Esel = 0,8809 – 0,0592 × 0
Esel = 0,8809 volt
Kunci Jawaban Soal OSP Kimia 2018 Nomer 18 yang sempurna D
Soal OSP Kimia 2018 Nomer 19
Selama elektrolisis air maritim dalam sel diafragma, dihasilkan gas klor, gas hidrogen dan natrium hidroksida. Rasio molar produk elektrolisis ini adalah:

Pembahasan Soal OSP Kimia 2018 Nomer 19
Rasio molar yaitu perbandingan jumlah mol tiap spesi(zat) yang terlibat dalam reaksi. Rasio molar sanggup dilihat pada koefisien setiap zat dalam reaksi yang setara.
Air maritim mengandung ion Na+, Cl– dan H2O. Bila larutan tersebut dielektrolisis maka yang terjadi adalah:
2H2O(l) + 2e– → 2OH–(aq) + H2(g)
2Cl–(aq) → Cl2(g) + 2e–
2H2O(l) + 2Cl–(aq) → 2OH–(aq) + H2(g) + Cl2(g)
Reaksi lengkapnya:
2H2O(l) + 2NaCl(aq) → 2NaOH(aq) + H2(g) + Cl2(g)
jadi rasio molar Cl2 : H2 : NaOH = 1 : 1 : 2
Kunci Jawaban Soal OSP Kimia 2018 Nomer 19 yang sempurna B
Soal OSP Kimia 2018 Nomer 20
Perhatikan sel volta berikut ini:
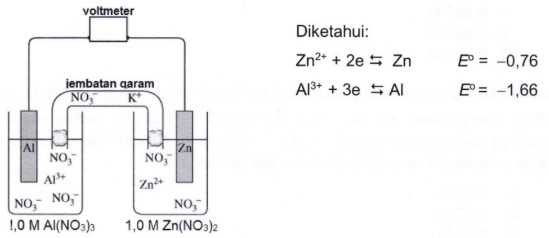
Jika sel volta tersebut digunakan, maka pernyataan yang benar adalah
A. Elektroda aluminium yaitu katoda dan elektroda zink yaitu anoda.
B. Elektron mengalir dari elektroda zink ke elektroda aluminium
C. Ion nitrat mengalir melalui jembatan garam ke larutan aluminium nitrat
D. Setengah reaksi yang terjadi di elektroda zink yaitu Zn → Zn2+ + 2e–
E. Elektroda aluminium dan zink beratnya tetap
Pembahasan Soal OSP Kimia 2018 Nomer 20
Agar reaksi sanggup berlangsung maka Al harus mengalami oksidasi (Al(s) → Al3+ (aq) + 3e– ). Al melarut dan massanya berkurang.
Zn harus mengalami reduksi (Zn2+(aq) + 2e– → Zn(s)). Zn massanya akan bertambah.
Oksidasi terjadi di anode, Al berperan sebagai anode. Reduksi terjadi di katoda, Zn berperan sebagai katoda.
Aliran elektron dari anode Al daerah elektron dilepaskan menuju katode Zn.
Karena Al3+ jumlahnya bertambah selama reaksi maka akan dinetralkan dengan ion nitrat yang mengalir melalui jembatan garam. Ion nitrat mengalir ke larutan Al(NO3)3.
Kunci Jawaban Soal OSP Kimia 2018 Nomer 20 yang sempurna C
Demikian tadi pembahasan soal OSP Kimia tahun 2018 untuk nomor 11-20. Nomor yang lain menyusul.
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 1-10
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 11-20
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 21-30
Pembahasan Soal OSP Kimia Tahun 2018 PDF Nomor 11-20
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon