Kesetimbangan Kimia
Dalam reaksi kimia, kesetimbangan kimia adalah keadaan dimana kedua reaktan dan produk hadir dalam konsentrasi yang tidak mempunyai kecenderungan lebih lanjut untuk berubah seiring berjalannya waktu.
Biasanya, keadaan ini terjadi ketika reaksi ke depan berlangsung pada laju yang sama dengan reaksi balik. Laju pada reaksi maju dan mundur umumnya tidak nol, tapi sama. Dengan demikian, tidak ada perubahan higienis dalam konsentrasi reaktan dan produk. Keadaan menyerupai ini dikenal sebagai kesetimbangan dinamis.
Untuk persamaan reaksi reversibel yang berada dalam kesetimbangan pada temperatur tertentu berikut:
aA + bB ⇌ cC +dD Tanda panah kesetimbangan kimia. Kesetimbangan Kimia – Reaksi Kimia – Termodinamika, Pengaruh Suhu, Zat murni, Jenis Kesetimbangan. Sumber foto: Wikimedia Commons
Tanda panah kesetimbangan kimia. Kesetimbangan Kimia – Reaksi Kimia – Termodinamika, Pengaruh Suhu, Zat murni, Jenis Kesetimbangan. Sumber foto: Wikimedia Commons
Sejarah Kesetimbangan Kimia

Buret, suatu peralatan laboratorium umum untuk melakukan titrasi, teknik eksperimental penting dalam kesetimbangan dan kimia analitik.
Konsep kesetimbangan kimia dikembangkan setelah Berthollet (1803) menemukan bahwa beberapa reaksi kimia bersifat reversibel
Untuk setiap adonan reaksi yang ada pada kesetimbangan, laju pada reaksi maju dan mundur yakni sama. Dalam persamaan berikut ini panah menunjuk kedua arah memperlihatkan kesetimbangan, A dan B yakni spesi reaktan kimia, S dan T yakni spesi produk, dan α, β, σ, dan τ adalah koefisien stoikiometri dari reaktan dan produk tersebut:
- α A + β B
 σ S + τ T
σ S + τ T
Posisi konsentrasi kesetimbangan dari suatu reaksi dikatakan berada “jauh ke kanan” jika, pada kesetimbangan, hampir semua reaktan dikonsumsi. Sebaliknya posisi kesetimbangan dikatakan “jauh ke kiri” jikalau hampir tidak ada produk yang terbentuk dari reaktan.
Guldberg dan Waage (1865), membangun gagasan Berthollet, mengusulkan hukum agresi massa:
dimana A, B, S dan T adalah massa aktif dan k+ serta k− adalah konstanta laju. Karena pada kesetimbangan, laju maju dan mundur yakni sama:
Dan rasio konstanta laju juga konstan, kini dikenal sebagai konstanta kesetimbangan kimia.
Berdasarkan konvensi, produk adalah pembilang.
Namun, hukum agresi massa hanya berlaku untuk reaksi satu tahap gabungan yang dilanjutkan melalui satu keadaan transisi dan tidak berlaku secara umum karena persamaan laju tidak, secara umum, mengikuti reaksi stoikiometri seperti Guldberg dan Waage telah usulkan (lihat, misalnya, substitusi nukleofilik oleh SN1atau reaksi hidrogen dan bromin untuk membentuk hidrogen bromida). Kesetaraan laju reaksi ke depan dan ke belakang, bagaimanapun, yakni syarat kondisi yang dibutuhkan untuk keseimbangan kimiawi, meskipun tidak cukup untuk menjelaskan mengapa kesetimbangan kimia terjadi.
Terlepas dari kegagalan derivasi ini, konstanta kesetimbangan kimia untuk sebuah reaksi memang konstan, terlepas dari kegiatan banyak sekali spesies yang terlibat, meskipun hal itu bergantung pada suhu menyerupai yang diamati oleh persamaan van ‘t Hoff.
Menambahkan katalis akan menghipnotis reaksi maju maupun reaksi sebaliknya dengan cara yang sama dan tidak akan besar lengan berkuasa pada konstanta kesetimbangan kimia. Katalis akan mempercepat kedua reaksi sehingga meningkatkan kecepatan di mana keseimbangan tercapai.
Meskipun konsentrasi kesetimbangan makroskopis konstan pada waktunya, reaksi terjadi pada tingkat molekul. Misalnya, dalam kasus asam asetat yang dilarutkan dalam air dan membentuk ion asetat dan hidronium,
- CH3CO2H + H2O ⇌ CH3CO−2 + H3O+
Sebuah proton sanggup melompat dari satu molekul asam asetat ke molekul air dan kemudian ke anion asetat untuk membentuk molekul asam asetat lain dan membiarkan jumlah molekul asam asetat tidak berubah. Ini yakni contoh kesetimbangan dinamis. Kesetimbangan, menyerupai sisa termodinamika, yakni fenomena statistik, rata-rata sikap mikroskopis.
Prinsip Le Châtelier (1884)
Memberi gambaran wacana sikap suatu sistem kesetimbangan dikala perubahan kondisi reaksinya terjadi. Jika kesetimbangan dinamis terganggu dengan mengubah kondisinya, posisi kesetimbangan bergerak untuk membalikkan sebagian perubahan. Misalnya, menambahkan lebih banyak S dari luar akan menjadikan kelebihan produk, dan sistem akan mencoba untuk melawannya dengan meningkatkan reaksi balik dan mendorong titik kesetimbangan ke belakang (meskipun konstanta kesetimbangan akan tetap sama).
Jika asam mineral ditambahkan ke dalam adonan asam asetat, meningkatkan konsentrasi ion hidronium, jumlah disosiasi harus berkurang dikala reaksi digerakkan ke kiri sesuai dengan prinsip ini. Hal ini juga sanggup disimpulkan dari verbal konstanta kesetimbangan untuk reaksi:
Jika {H3O+} bertambah {CH3CO2H} harus bertambah dan CH3CO−2 harus berkurang. H2O dilepaskan, sebab pelarut dan konsentrasinya tetap tinggi dan hampir konstan.
Versi kuantitatif diberikan oleh hasil bagi reaksi.
J. W. Gibbs menyarankan pada tahun 1873 bahwa kesetimbangan tercapai saat energi bebas Gibbs dari sistem bernilai minimum (dengan anggapan reaksi dilakukan pada suhu dan tekanan konstan)
Apa artinya ini yakni turunan dari energi Gibbs berkenaan dengan koordinat reaksi (ukuran reaksi yang telah terjadi, mulai dari nol untuk semua reaktan hingga maksimum untuk semua produk) lenyap, menerangkan titik stasioner.
Turunan ini disebut reaksi energi Gibbs (atau perubahan energi) dan sesuai dengan perbedaan antara potensial kimia dari reaktan dan produk pada komposisi adonan reaksi.Kriteria ini dibutuhkan dan cukup. Jika adonan tidak berada pada kesetimbangan kimia, pembebasan kelebihan energi Gibbs (atau energi bebas Helmholtz pada volume reaksi konstan) yakni “kekuatan penggerak” untuk komposisi adonan biar berubah hingga tercapai kesetimbangan. Konstanta kesetimbangan sanggup dikaitkan dengan energi bebas Gibbs standar untuk reaksi dengan persamaan
Dimana R adalah tetapan gas ideal dan T adalah suhu.
Bila reaktan dilarutkan dalam medium dengan kekuatan ion tinggi; hasil koefisien aktivitas dapat dianggap konstan. Dalam hal ini hasil bagi konsentrasi, Kc,
dimana [A] adalah konsentrasi A, dan lain-lain, tidak bergantung pada konsentrasi analitis reaktan. Untuk alasan ini, konstanta kesetimbangan untuk larutan biasanya ditentukan di media dengan kekuatan ion tinggi. Kc bervariasi dengan kekuatan ion, suhu dan tekanan (atau volume). Juga Kp untuk gas bergantung pada tekanan parsial.
Termodinamika
Pada suhu dan tekanan konstan, harus mempertimbangkan energi bebas Gibbs, G, sedangkan pada suhu dan volume konstan, harus mempertimbangkan energi bebas Helmholtz: A, untuk reaksinya; dan pada energi dalam dan volume konstan, seseorang harus mempertimbangkan entropi untuk reaksi: S.
Kasus volume konstan penting dalam geokimia dan kimia atmosfer di mana variasi tekanan signifikan. Perhatikan bahwa, jikalau reaktan dan produk berada dalam keadaan standar (benar-benar murni), maka tidak akan ada reversibilitas dan tidak ada kesetimbangan. Memang, mereka tentu saja harus menempati kisi-kisi ruang. Pencampuran produk dan reaktan berkontribusi pada entropi besar (dikenal sebagai entropi pencampuran) pada keadaan yang mengandung adonan produk dan reaktan yang sama. Perubahan energi Gibbs standar, bersamaan dengan energi pencampuran Gibbs, memilih keadaan kesetimbangan.
Pada artikel ini hanya kasus tekanan konstan yang dipertimbangkan. Hubungan antara energi bebas Gibbs dan konstanta kesetimbangan sanggup ditemukan dengan mempertimbangkan potensial kimia.
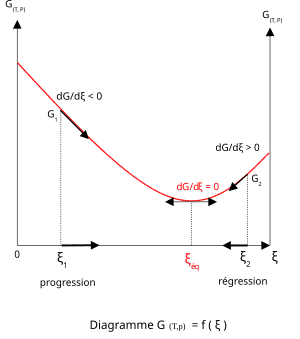
Pada suhu dan tekanan konstan, energi bebas Gibbs, G, sebab reaksinya hanya bergantung pada tingkat reaksi.: ξ (huruf Yunani xi), dan hanya sanggup berkurang sesuai dengan hukum kedua termodinamika. Artinya turunan dari G dengan ξ harus negatif jikalau reaksi terjadi; pada kesetimbangan turunannya sama dengan nol.
- :
kesetimbangan
Untuk memenuhi kondisi kesetimbangan termodinamika, energi Gibbs harus stasioner, yang berarti bahwa turunan dari G berkenaan dengan tingkat reaksi: ξ, harus nol. Dapat ditunjukkan bahwa dalam masalah ini, jumlah potensial kimia dari produk sama dengan jumlah yang sesuai dengan reaktan. Oleh sebab itu, jumlah energi Gibbs dari reaktan harus sama dengan jumlah energi Gibbs dari produk.
dimana μ Dalam hal ini yakni energi Gibbs molar parsial, sebuah potensial kimia. Potensial kimia pereaksi A yakni fungsi aktivitas, {A} dari pereaksi tersebut.
(dimana μoA adalah potensial kimia standar).
Definisi persamaan energi bebas Gibbs berinteraksi dengan hubungan termodinamika fundamental untuk menghasilkan
- .
Memasukkan dNi = νi dξ kedalam persamaan di atas menghasilkan koefisien stoikiometri ({\displaystyle \nu _{i} }) dan diferensial yang memperlihatkan reaksi terjadi sekali (dξ). Pada tekanan dan suhu konstan, persamaan di atas sanggup ditulis sebagai
- yang merupakan perubahan energi bebas Gibbs bagi reaksi .
Hal ini menghasilkan:
- .
Dengan mensubstitusi potensial kimia:
- ,
hubungannya menjadi:
- :
yaitu perubahan energi Gibbs standar bagi reaksi yang sanggup dihitung memakai tabel termodinamika. Hasil bagi reaksinya didefinisikan sebagai:
Karenanya,
Pada kesetimbangan:
mengarah pada:
dan
menghasilkan nilai perubahan energi Gibbs standar, memungkinkan perhitungan konstanta kesetimbangan.
Pengaruh Suhu Kesetimbangan Kimia
Pengaruh perubahan suhu pada konstanta kesetimbangan diberikan oleh persamaan van ‘t Hoff
Karenanya, untuk reaksi eksotermik (ΔH adalah negatif), K menurun dengan kenaikan suhu, namun untuk reaksi endotermik, (ΔH positif) K meningkat dengan kenaikan suhu. Rumus alternatifnya adalah
Pada pandangan pertama ini sepertinya memperlihatkan cara untuk mendapatkan entalpi molar standar reaksi dengan mempelajari variasi K dengan suhu. Namun, dalam praktiknya, metode ini tidak sanggup mendapatkan amanah sebab propaganda kesalahan hampir selalu mengatakan kesalahan yang sangat besar pada nilai yang dihitung dengan cara ini.
Zat Murni Keseimbangan Kimia
Bila zat murni (cairan atau padatan) dilibatkan dalam kesetimbangan, aktivitasnya tidak muncul dalam konstanta kesetimbangan. Karena nilai numerik mereka dianggap satu.
Menerapkan rumus umum untuk konstanta kesetimbangan pada masalah spesifik larutan encer asam asetat dalam air diperoleh
- CH3CO2H + H2O
 CH3CO2− + H3O+
CH3CO2− + H3O+
Untuk semua larutan yang sangat terkonsentrasi, air dapat dianggap sebagai cairan “murni”, dan sebab itu mempunyai kegiatan satu. Ekspresi konstanta kesetimbangan oleh sebab itu biasanya ditulis sebagai
- .
Kasus tertentu adalah swaionisasi air itu sendiri
- 2 H2O
 H3O+ + OH−
H3O+ + OH−
Karena air yakni pelarut, dan mempunyai kegiatan satu, konstanta swaionisasi air didefinisikan sebagai
Sangat sah untuk menulis [H+] untuk konsentrasi ion hidronium, sebab keadaan solvasi proton konstan (dalam larutan encer) dan risikonya tidak menghipnotis konsentrasi kesetimbangan. Kw bervariasi dengan variasi kekuatan ion dan/atau suhu.
Konsentrasi H+ dan OH− bukanlah kuantitas independen. Umumnya [OH−] digantikan oleh Kw[H+]−1 dalam persamaan konstanta kesetimbangan yang dinyatakan meliputi ion hidroksida.
Padatan juga tidak muncul dalam verbal konstanta kesetimbangan, jikalau dianggap murni dan dengan demikian kegiatan mereka menjadi satu. Contohnya adalah reaksi Boudouard:
dimana persamaan (tanpa karbon padat) ditulis sebagai:
Jenis Kesetimbangan Kimia
- N2 (g)
 N2 (diserap)
N2 (diserap) - N2 (diserap)
 2 N (diserap)
2 N (diserap) - H2 (g)
 H2 (diserap)
H2 (diserap) - H2 (diserap)
 2 H (diserap)
2 H (diserap) - N (diserap) + 3 H(diserap)
 NH3 (diserap)
NH3 (diserap) - NH3 (diserap)
 NH3 (g)
NH3 (g)
- Dalam fasa gas: mesin roket
- Sintesis industri seperti amonia dalam proses Haber–Bosch (digambarkan di sebelah kanan) terjadi melalui serangkaian langkah kesetimbangan termasuk proses adsorpsi.
- Kimia atmosfer
- Air maritim dan air alami lainnya: oseanografi kimia
- Distribusi antara dua fase
- Koefisien distribusi log D: penting untuk obat-obatan di mana lipofilisitas yakni sifat yang signifikan dari obat
- Ekstrasi cair-cair, pertukaran ion, kromatografi
- Kelarutan produk
- Serapan dan pelepasan oksigen dengan hemoglobin dalam darah
- Kesetimbangan asam-basa: konstanta disosiasi asam, hidrolisis, larutan penyangga, indikator, homeostasis asam-basa
- Kompleksitas pengikat logam: agen pelacak, terapi kelasi, agen pengontras MRI, kesetimbangan Schlenk
- Pembentukan aduk: kimia pembawa tamu, kimia supramolekuler, pengenalan molekul, dinitrogen tetroksida
- Dalam reaksi berosilasi tertentu, pendekatan terhadap kesetimbangan tidak asimtotik tetapi dalam bentuk osilasi teredam.[7]
- Persamaan Nernst yang terkait dalam elektrokimia memberi perbedaan potensial elektroda sebagai fungsi konsentrasi redoks.
- Ketika molekul di setiap sisi kesetimbangan sanggup bereaksi lebih lanjut secara ireversibel dalam reaksi sekunder, rasio produk selesai ditentukan sesuai dengan prinsip Curtin–Hammett.
Dalam aplikasi ini, istilah menyerupai konstanta kestabilan, konstanta pembentukan, konstanta pengikatan, konstanta afinitas, konstanta asosiasi/disosiasi digunakan. Dalam biokimia, yakni umum untuk memberi unit konstanta pengikatan, yang berfungsi untuk memilih unit konsentrasi yang dipakai bila nilai konstanta ditentukan.
Soal dan Jawaban Kesetimbangan Kimia
1. Tentukan persamaan tetapan kesetimbangan (Kc) dari sistem kesetimbangan berikut ini:

Jawaban:
Perhatikan rumus untuk kesetimbangan kimia berikut ini:Sehingga
2. Dalam wadah 1 liter terjadi reaksi kesetimbangan

dengan harga Kc = 0,5 pada suhu tertentu. Konsentrasi I2 yang dibutuhkan biar dikala kesetimbangan terdapat P M H2 dan Q M HI adalah….
Jawaban:
Tetapan kesetimbangan untuk reaksi di atas
Masukkan datanya sehingga:
3. Pada temperatur 430°C, tetapan kesetimbangan Kc untuk reaksi H2(g) + I2(g) ⇌ 2HI(g) yakni 54,3. Diketahui pada eksperimen dengan temperatur yang sama, konsentrasi awal H2, I2, dan HI berturut-turut yakni 0,00623 M, 0,00414 M, dan 0,0224 M. Hitunglah konsentrasi masing-masing spesi pada keadaan setimbang.
Jawaban:
[H2]0 = 0,00623 M
[I2]0 = 0,00414 M
[HI]0 = 0,0224 M
Kc = 54,3
Pertama, kita tentukan nilai kuosien reaksi, Qc, untuk mengetahui apakah sistem telah setimbang atau belum, dan ke arah mana reaksi berlangsung jikalau belum setimbang.

Karena Qc (19,5) < Kc (54,3), reaksi akan berlangsung dari arah kiri ke kanan hingga mencapai kesetimbangan. Jadi, konsentrasi H2 dan I2 akan berkurang dan konsentrasi HI akan bertambah hingga reaksi setimbang.
Selanjutnya, asumsikan bahwa konsentrasi H2 berkurang sebanyak x hingga reaksi setimbang, kemudian kita buat persamaan stoikiometri dengan MRS (Mula-mula, Reaksi, Setimbang).


Dengan menyelesaikan persamaan kuadrat dalam bentuk dengan rumus
diperoleh: x = 0,0114 M atau x = 0,00156 M.
Penyelesaian x = 0,0114 M mustahil sebab nilainya lebih besar dari konsentrasi awal H2 dan I2. Jadi, penyelesaian yang benar yakni x = 0,00156 M.
Jadi, pada kesetimbangan kimia tersebut, konsentrasi masing-masing spesi yaitu:

Bacaan Lainnya
- Entalpi Termokimia – Pemanasan / Kalor Fisika – Soal dan Jawaban
- Termokimia – Rumus, Penjelasan Beserta Contoh Soal dan Jawaban
- Tabel Periodik Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna dan Jenis
- Unsur, Senyawa dan Campuran Kimia – Beserta Penjelasan & Rumus
- Rumus Fisika: Alat optik: Lup, Mikroskop, Teropong Bintang, Energi, Frekuensi, Gaya, Gerak, Getaran, Kalor, Massa jenis, Medan magnet, Mekanika fluida, Momen Inersia, Panjang gelombang, Pemuaian, Percepatan (akselerasi), Radioaktif, Rangkaian listrik, Relativitas, Tekanan, Usaha Termodinamika, Vektor
- Bagaimana Albert Einstein mendapatkan rumus E=mc² ?
- Cara Mengemudi Aman Pada Saat Mudik atau Liburan Panjang
- Jenis Virus Komputer – Cara Gratis Mengatasi Dengan Windows Defender
- Cara Menghentikan Penindasan Bullying
- Cara menjaga keluarga Anda kondusif dari t3r0ris – Ahli anti-teror menerbitkan panduan praktis
- Apakah Anda Memerlukan Asuransi Jiwa? – Cara Memilih Asuransi Jiwa Untuk Pembeli Yang Pintar
- 10 Cara Memotivasi Anak Untuk Belajar Agar Menjadi Pintar
- Daftar Jenis Kanker: Pemahaman Kanker, Mengenal Dasar-Dasar, Contoh Kanker, Bentuk, Klasifikasi, Sel dan Pemahaman Penyakit Kanker Lebih Jelas
- Penyebab Dan Cara Mengatasi Iritasi Atau Lecet Akibat Pembalut Wanita
- Sistem Reproduksi Manusia, Hewan dan Tumbuhan
- Cara Mengenal Karakter Orang Dari 5 Pertanyaan Berikut Ini
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?

Apakah Anda mempunyai sesuatu untuk dijual, disewakan, layanan apa saja yang ditawarkan atau lowongan pekerjaan? Pasang iklan & promosikan jualan atau jasa Anda kini juga! 100% GRATIS di: www.TokoPinter.com

3 Langkah super mudah: tulis iklan Anda, beri foto & terbitkan! semuanya di Toko Pinter
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jikalau Anda mengunduh aplikasi kita!
Siapa bilang mau pandai harus bayar? Aplikasi Ilmu pengetahuan dan warta yang menciptakan Anda menjadi lebih smart!
Sumber bacaan: Libretexts
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz |Matematika|IPA | Geografi & Sejarah|Info Unik|Lainnya
Sumber aciknadzirah.blogspot.com





























EmoticonEmoticon