Pembahasan Soal OSN Kimia 2016 Tingkat Kabupaten (OSK) PDF – Dalam mempersiapkan seleksi Olimpiade Sains Nasional tingkat Kabupaten / Kota (OSK), perlu adanya pembahasan soal-soal OSK tahun sebelumnya. Dari panitia OSN, biasanya yang dirilis yaitu kunci tanggapan pilihan ganda (pilgan) dan pembahasan soal essay saja tanpa bahasa pilgan. Perlu adanya pembahasan khusus soal pilihan ganda. Dalam kesempatan kali ini, merupakan pembahasan soal OSK Kimia 2016 format PDF.
Pembahasan Soal OSN Kimia 2016 Tingkat Kabupaten (OSK) PDF
Sebelum lanjut, baca juga :
Pembahasan Soal OSK Kimia 2017 PDF
Pembahasan Soal OSK Kimia 2018 PDF
BACA JUGA : Pembahasan Soal OSK Kimia 2019 PDF
Soal OSK Kimia 2016 PDF Nomer 1
Larutan kalium permanganat direaksikan dengan kalium oksalat dalam suasana basa menghasilkan mangan oksida (MnO2) dan karbon dioksida. Maka koefisien kalium permanganat dan kalium oksalat sehabis reaksi setara yaitu:
A. 4 dan 2
B. 2 dan 3
C. 3 dan 2
D. 2 dan 6
E. 4 dan 8
Pembahasan Soal OSK Kimia 2016 PDF Nomer 1
Persamaan reaksi: KMnO4 + K2C2O4 → MnO2 + CO2
MnO4– + 2H2O + 3e– → MnO2 + 4OH–
C2O42– → 2CO2 + 2e–
2MnO4– + 4H2O + 6e– → 2MnO2 + 8OH–
3C2O42– → 6CO2 + 6e–
2MnO4– + 4H2O + 3C2O42– → 2MnO2 + 8OH– + 6CO2
2KMnO4 + 3K2C2O4 + 4H2O → 2MnO2 + 8KOH + 6CO2
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 1 yaitu B
Soal OSK Kimia 2016 PDF Nomer 2
Di antara larutan aqueous pada pilihan A, B, C, D dan E berikut, larutan aqueous yang sanggup bereaksi dengan logam magnesium adalah:
A. Ammonia, NH3
B. Kalium hidroksida, KOH
C. Hidrogen klorida, HCl
D. Natrium hidrogenkarbonat
E. Semua larutan di atas (pada pilihan A, B, C dan D) sanggup bereaksi dengan Mg
Pembahasan Soal OSK Kimia 2016 PDF Nomer 2
Mg termasuk logam alkali tanah yang relatif gampang melepaskan elektron membentuk kation Mg2+.
Reaksi ibarat pada soal ini yaitu reaksi penggantian kation.
Perhatikan deret volta, maka akan nampak terang posisi Mg → Li K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi Cu Hg Ag Pt Au, M
Mg terang akan dengan gampang mereposisi H dalam HCl alasannya yaitu Mg yaitu reduktor yg baik bagi H, tidak demikian dengan K dan Na. Untuk NH3?
Bisa juga alasannya yaitu dalam larutan basah yang bersifat basa Mg sulit bereaksi alasannya yaitu aksara Mg juga akan membentuk basa dalam larutan tersebut. Sementara dalam larutan HCl yang tentu saja bersifat asam Mg akan dengan gampang membentuk garam MgCl2. Mungkin begitu.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 2 yaitu C
Soal OSK Kimia 2016 PDF Nomer 3
Bila gelembung gelembung gas klorin dialirkan ke dalam larutan natrium hidroksida pekat panas, akan terbentuk larutan:
A. NaCl dan NaClO
B. NaCl dan NaClO3
C. NaClO dan NaClO3
D. NaClO saja
E. NaClO3 saja
Pembahasan Soal OSK Kimia 2016 PDF Nomer 3
Reaksi Gas klorin dengan NaOH pekat panas ini merupakan reaksi disproporsionasi, bilangan oksidasi Cl mengalami penurunan (dari Cl2 → 2Cl–), sekaligus mengalami kenaikan (dari Cl2 → ClO3–)
6NaOH + 3Cl2 → 5NaCl + NaClO3 + 3H2O
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 3 yaitu B
Soal OSK Kimia 2016 PDF Nomer 4
Reaksi berikut ini, manakah yang merupakan reaksi redoks ?
a. K2CrO4 (aq) + BaCl2(aq) → BaCrO4 + 2KCl(aq)
b. Na(s) +H2O (l) → NaOH + H2 (g)
c. Pb2+ (aq) + 2Br– (aq) → PbBr2(s)
d. Cu(s) + S(s) → CuS
A. Hanya a dan c
B. Hanya a, b dan c
C. Hanya b, c dan d
D. Hanya b dan d
E. semuanya yaitu reaksi redoks
Pembahasan Soal OSK Kimia 2016 PDF Nomer 4
Salah satu ciri reaksi redoks yang kasat mata yaitu reaksi unsur membentuk senyawa atau sebaliknya, dengan begitu sudah niscaya terjadi perubahan bilangan oksidasi. Yang sesuai dengan ciri ini yaitu b dan d sedangkan a dan c yaitu reaksi kimia biasa, tidak terjadi perubahan bilangan oksidasi.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 4 yaitu D
Soal OSK Kimia 2016 PDF Nomer 5
Setengah reaksi yang terjadi di anoda dalam persamaan berikut:
3MnO4– (aq) + 24H+ (aq) + 5Fe(s) → 3Mn+2 (aq) + 5Fe+3 (aq) + 12H2O (l) adalah
A. Fe+2(aq) → Fe+3(aq) + e–
B. MnO4– (aq) + 8H+ (aq) + 5e– → Mn+2 (aq) + 4H2O (l)
C. Fe(s) → Fe+3(aq) + 3e–
D. 2MnO4– (aq) + 12H+ (aq) + 6e- → 2Mn+2(aq) + 3H2O (l)
E. Fe (s) → Fe+2 (aq) + 2e–
Pembahasan Soal OSK Kimia 2016 PDF Nomer 5
Dalam reaksi redoks, di anoda terjadi reaksi oksidasi, bilangan oksidasi suatu spesi akan meningkat. Pada soal ini reaksi oksidasi yaitu Fe(s) → Fe+3(aq) + 3e–
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 5 yaitu C
Soal OSK Kimia 2016 PDF Nomer 6
Sebanyak 2 gram sampel gas hidrogen (1H1) pada temperatur T dan volume V memberikan tekanan P. Gas deuterium, 1H2, yaitu suatu isotop dari hidrogen.
Berikut ini, kondisi manakah yang juga akan memperlihatkan tekanan sebesar P pada temperatur T yang sama?
A. 2 g deuterium volume V
B. 4 g deuterium volume V/2
C. Campuran 1 g hidrogen dan 2 g deuterium dengan total volume V.
D. Campuran 2 g hidrogen dan 1 g deuterium dengan total volume 2V.
E. Campuran 2 g hidrogen dan 2 g deuterium dengan total volume 2V.
Pembahasan Soal OSK Kimia 2016 PDF Nomer 6
2 g gas H2 = 2 g : 2 g/mol = 1 mol = n
→ PV = nRT → PV = RT → (RT)/P = V
2 g gas H2 dari deutrium = 2 g : 4 g/mol = 2 mol
→ PV = 2RT → (RT)/P = V/2
4 g gas H2 dari deutrium = 4 g : 4 g/mol = 1 mol
→ PV = RT → (RT)/P = V
1 g gas H2 dari hidrogen = 1 g : 2 g/mol = 0,5 mol
2 g gas H2 dari deutrium = 2 g : 4 g/mol = 0,5 mol
Total adonan ini sebanyak 1 mol
→ PV = RT → (RT)/P = V
2 g gas H2 dari hidrogen = 2 g : 2 g/mol = 1 mol
1 g gas H2 dari deutrium = 1 g : 4 g/mol = 0,25 mol
Total adonan ini sebanyak 1,25 mol
→ PV = 1,25.RT → (RT)/P = V/1,25
2 g gas H2 dari hidrogen = 2 g : 2 g/mol = 1 mol
2 g gas H2 dari deutrium = 2 g : 4 g/mol = 0,5 mol
Total adonan ini sebanyak 1,5 mol
→ PV = 1,5.RT → (RT)/P = V/1,5
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 6 yaitu C
Soal OSK Kimia 2016 PDF Nomer 7
Berikut ini yaitu alur nilai PV/RT terhadap P, untuk gas ideal dan gas non-ideal.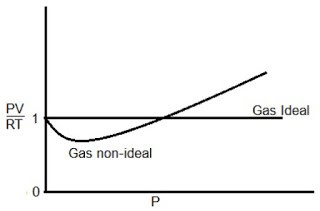
P yaitu tekanan gas, V yaitu volume gas, R yaitu tetapan gas ideal dan T yaitu temperatur. Dari gas gas berikut ini, manakah yang memperlihatkan deviasi (penyimpangan) paling besar dari sifat gas ideal?
A. Helium
B. Nitrogen
C. Metana
D. Etena
E. Ammonia
Pembahasan Soal OSK Kimia 2016 PDF Nomer 7
Pada gas ideal interaksi antarmolekul dianggap tidak ada atau nol. Semakin besar lengan berkuasa interaksi antarmolekul berarti akan semakin menyimpang dari gas ideal. Pada pilihan yang tersedia hampir semua zat bersifat non polar, kecuali ammonia. Amonia memang bersifat polar dan juga mempunyai ikatan hidrogen, dengan demikian ammonia akan mengalami penyimpangan paling besar dibanding sifat gas ideal.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 7 yaitu E
Soal OSK Kimia 2016 PDF Nomer 8
Diantara senyawa berikut ini, manakah yang mempunyai tekanan uap paling rendah:
A. Air, H2O
B. Hidrogenperoksida, H2O2
C. Etanol, CH3CH2OH
D. Aseton, CH2CO-CH2
E. Asam asetat, CH3COOH
Pembahasan Soal OSK Kimia 2016 PDF Nomer 8
Struktur H2O2 adalah H-O-O-H yang menghasilkan ikatan hidrogen lebih besar daripada air dan jauh lebih bersifat polar dibanding pilihan lain yang tersedia. Dengan demikian kekuatan antarmolekul lebih besar lengan berkuasa dalam H2O2 yang menghasilkan titik didih normal yang lebih tinggi untuk H2O2 dan tekanan uap yang lebih rendah.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 8 yaitu B
Soal OSK Kimia 2016 PDF Nomer 9
Dibandingkan dengan air murni, larutan NaCl 0,1 mol/L mempunyai:
A. pH lebih tinggi
B. Daya hantar listrik lebih rendah
C. Titik didih lebih rendah
D. Titik beku lebih rendah
E. Tekanan uap lebih tinggi
Pembahasan Soal OSK Kimia 2016 PDF Nomer 9
Larutan NaCl 0,1 mol/L mempunyai:
pH dianggap sama dengan air, daya hantar listrik yang lebih tinggi dibanding air, titik didih yang relatif lebih tinggi dan titik beku yang lebih rendah serta tekanan uapnya akan lebih rendah dibanding air alasannya yaitu sifat koligatifnya.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 9 adalah
Soal OSK Kimia 2016 PDF Nomer 10
Perhatikanlah unsur-unsur dalam susunan bersiklus yang terdapat dalam perioda ke 2 dari blok-p. Energi ionisasi pertama dari unsur-unsur ini adalah:
A. Naik dari B ke Ne
B. Turun dari B ke Ne
C. Naik dari B ke O, turun untuk F, dan lalu naik untuk Ne
D. Turun dari B ke N dan naik beraturan dari N ke Ne
E. Naik dari B ke N, turun untuk O dan naik dari O ke Ne
Pembahasan Soal OSK Kimia 2016 PDF Nomer 10
Berikut ini yaitu data faktual untuk nilai energi ionisasi pertama unsur periode ke-2 blok p.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 10 yaitu E
Soal OSK Kimia 2016 PDF Nomer 11
Berikut ini mengenai radius ion, berturut turut: F–, N–3 , P–3, S–2 . Urut-urutan yang benar mengenai radius ion tersebut adalah:
A. Radius F– > N–3 > P–3 > S–2
B. Radius S–2 > P–3 > N–3 >F–
C. Radius P–3 > N–3 > S–2 > F–
D. Radius P–3 > S–2 > N–3 > F–
E. Radius N–3 > S–2 > F– > P–3
Pembahasan Soal OSK Kimia 2016 PDF Nomer 11
Semua mengenai anion, ion yang bermuatan negatif, atom yang mendapatkan elektron.
Dalam satu periode sistem periodik unsur, semakin banyak elektron yang diterima dari luar semakin lemah kontrol dari inti sehingga jari-jari ionnya semakin besar.
P dan S seperiode (periode-3), sehingga jari-jari P–3 > S–2
N dan F seperiode (periode-2, sehingga jari-jari N–3 > F–
Pengaruh jumlah kulit (periode) lebih besar dibanding faktor jumlah elektron yang diterima, semakin besar periode semakin besar pula jari-jari anion. Kaprikornus jari-jari (radius) P–3 > S–2 > N–3 > F–
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 11 yaitu D
Soal OSK Kimia 2016 PDF Nomer 12
Di antara kelompok molekul di bawah ini yang tidak mengikuti kaidah oktet adalah
A. CO2, NH3, N2
B. O2, CO3–2, CH3Cl
C. BCl3, NO2, SO2
D. N2O4, HCN, NH4+
E. C2N2, ClNO2, CS2
Pembahasan Soal OSK Kimia 2016 PDF Nomer 12
Yang dimaksud soal ini yaitu molekul dengan atom pusat yang tidak mengikuti kaidah oktet. Kaidah oktet yaitu hukum bahwa atom akan stabil bila di sekitarnya terdapat 8 elektron. Ini akan menjadi terang bila molekul-molekul itu digambar struktur Lewisnya.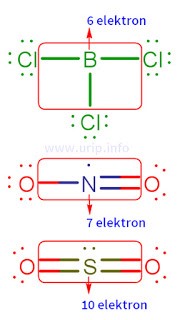
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 12 yaitu C
Soal OSK Kimia 2016 PDF Nomer 13
Berikut ini, kelompok mana yang hanya mengandung molekul ikatan kovalen?
A. Al, O3, As4
B. BCl3, SiCl4, PCl3
C. Cl2, NaCl, H2O
D. I2, H2S, NaI
E. NH4Br, N2H4, HBr
Pembahasan Soal OSK Kimia 2016 PDF Nomer 13
Secara kasat mata molekul yang berikatan kovalen biasa tersusun dari atom-atom nonlogam yang tidak berasal dari ionnya. Unsur-unsur nonlogam antara lain : B-Si-C-Sb-As-P-N-H-Te-Se-S-I-Br-Cl-O-F. Alternatif tanggapan yang sempurna yaitu BCl3, SiCl4, PCl3
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 13 yaitu B
Soal OSK Kimia 2016 PDF Nomer 14
Dari senyawa berikut ini, manakah yang kelompok zat mengandung ikatan hidrogen?
A. NH4Cl(s), NH3 (l), dan HNO3(l)
B. NH3(l), CH3NH2(l), dan HNO3(l)
C. NH4Cl(s), CH3NH2(l), dan HNO3(l)
D. NH4Cl(s) dan NH3(l)
E. NH4Cl(s) dan CH3NH2(l)
Pembahasan Soal OSK Kimia 2016 PDF Nomer 14
Zat-zat yang dalam bentuk padatan mustahil mengandung ikatan hidrogen. Zat dengan atom pusat N atau O atau F dan masih terdapat pasangan elektron bebas dan atom ligannya mengandung hidrogen maka akan mengandung ikatan hidrogen. Jawaban yang sempurna yaitu NH3(l), CH3NH2(l), dan HNO3(l)
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 14 yaitu B
Soal OSK Kimia 2016 PDF Nomer 15
Ikatan apa yang terdapat dalam cis-2-butena berikut ini: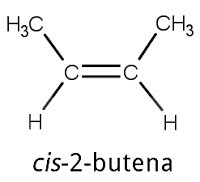
A. 9 ikatan- dan 3 ikatan-π
B. 10 ikatan-dan 2 ikatan-π
C. 11 ikatan-dan 1 ikatan-π
D. 12 ikatan- dan 1 ikatan-π
E. 12 ikatan-
Pembahasan Soal OSK Kimia 2016 PDF Nomer 15
Setiap ikatan tunggal yaitu ikatan-
Setiap ikatan rangkap dua terdiri 1 ikatan- dan 1 ikatan-π
Setiap ikatan rangkap tiga terdiri 1 ikatan- dan 2 ikatan-π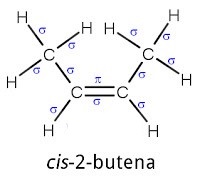
Pada molekul cis-2-butena terdapat:
10 ikatan tunggal = 10 ikatan-
1 ikatan rangkap dua = 1 ikatan- dan 1 ikatan-π
Jadi semua ikatan = 11 ikatan- dan 1 ikatan-π
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 15 yaitu C
Pembahasan Soal OSN Kimia 2016 Tingkat Kabupaten (OSK) PDF
Soal OSK Kimia 2016 PDF Nomer 16
Untuk reaksi berikut ini:
2 P(s) + 3 Cl2(g) → 2 PCl3(g) DH = -574 kJ
Berapa mol fosfor yang diharapkan untuk menghasilkan panas sebanyak 488 kJ?
A. 0,85 mol P
B. 1,20 mol P
C. 1,70 mol P
D. 2,35 mol P
E. 3,40 mol P
Pembahasan Soal OSK Kimia 2016 PDF Nomer 16
2 mol P akan menghasilkan energi sebesar 574 kJ
x mol P akan menghasilkan energi sebesar 488 kJ
2 mol : x mol = 574 kJ : 488 kJ
x = (2 mol × 488 kJ) : 574 kJ
x = 1,70 mol
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 16 yaitu C
Soal OSK Kimia 2016 PDF Nomer 17
Perhatikan proses reaksi berikut ini:
2A→ ½B + C ΔH = 5 kJ/mol
3/2B + 4C → 2A + C + 3D ΔH = -15 kJ/mol
E + 4A → C ΔH = 10 kJ/mol
Hitunglah ΔH untuk reaksi : C → E + 3D
A. 0 kJ/mol
B. -20 kJ/mol
C. 10 kJ/mol
D. 20 kJ/mol
E. -10 kJ/mol
Pembahasan Soal OSK Kimia 2016 PDF Nomer 17
Pastikan zat yang bersesuaian ada pada ruas yang sama sesuai dengan reaksi yang akan ditentukan nilai ∆H-nya.
Jumlah reaksi harus menghasilkan persamaan sebagaimana ditentukan, yaitu C → E + 3D
C harus di ruas kiri, E dan D harus ada di ruas kanan.
Membalik persamaan berarti mengalikan tanda ∆H dengan -1.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 17 yaitu E
Soal OSK Kimia 2016 PDF Nomer 18
Zat R sanggup bereaksi membentuk produk P1 atau produk P2. Profil reaksi untuk dua reaksi tersebut ditunjukkan di bawah ini: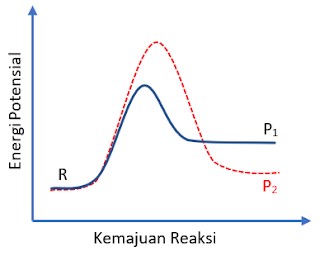
Dibandingkan dengan reaksi R → P1, reaksi R → P2 adalah:
A. Lebih cepat dan kurang endotermis
B. Lebih cepat dan sangat eksotermis
C. Lebih cepat dan lebih endotermis
D. Lebih lambat dan kurang endotermis
E. Lebih lambat dan lebih endotermis
Pembahasan Soal OSK Kimia 2016 PDF Nomer 18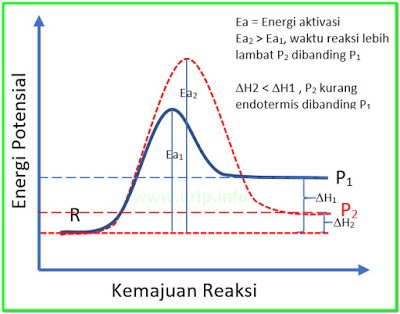
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 18 yaitu D
Soal OSK Kimia 2016 PDF Nomer 19
Dalam larutan aqueous, ion peroksidisulfat (S2O8–2) bereaksi dengan ion iodida sesuai reaksi berikut ini:
S2O8–2 (aq) + 3I– → 2SO4–2 (aq) + I3– (aq)
Suatu larutan yang disiapkan dengan komposisi 0,050 M ion S2O8–2 dan 0,072 M ion I–, dan kemajuan reaksi diamati dengan mengukur [I–]. Diperoleh data ibarat pada Tabel berikut: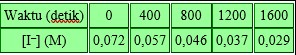
Konsentrasi S2O8–2 yang tersisa pada ketika 800 detik adalah
A. 0,015 M
B. 0,041 M
C. 0,076 M
D. 0,004 M
E. 0,046 M
Pembahasan Soal OSK Kimia 2016 PDF Nomer 19
S2O8–2 (aq) + 3I– → 2SO4–2 (aq) + I3– (aq)
Secara stoikiometri 1 mol S2O8–2 yang bereaksi setara dengan 3 mol I–, dan alasannya yaitu volume dalam sistem sama maka sanggup dinyatakan sebagai [S2O8–2] = 3 [I–] atau [I–] = ⅓ [S2O8–2]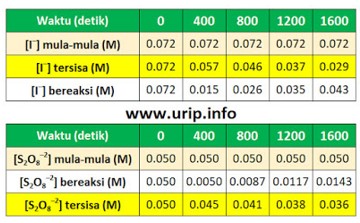
Setelah 800 detik (seperti pada tabel), I– yang tersisa yaitu 0,046 M, ini berarti I– yang bereaksi yaitu 0,026 M (didapat dari 0,072 M – 0,046 M).
Dengan demikian S2O8–2 yang bereaksi yaitu sebanyak 1/3 × 0,026 M atau 0,00867 M.
Jadi S2O8–2 yang tersisa = (0,050 – 0,0087) M = 0,0413 M
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 19 yaitu B
Soal OSK Kimia 2016 PDF Nomer 20
Dua gas diatom, X2 dan Y2 bereaksi sesuai persamaan berikut :
X2(g) + Y2(g) → 2XY(g).
Suatu adonan X2 dan Y2 masing-masing mengandung 0,5 mol dan dipanaskan dalam wadah tertutup hingga reaksi mencapai kesetimbangan. Grafik berikut ini memperlihatkan relasi antara jumlah mol masing-masing gas dan perubahan waktu.
Berdasarkan grafik di atas, berapa nilai konstanta kesetimbangan, Kc, untuk reaksi ini?
A. 1,5
B. 3
C. 9
D. 12
E. 18
Pembahasan Soal OSK Kimia 2016 PDF Nomer 20
Grafik di atas sanggup pula diterjemahkan ibarat tabel berikut: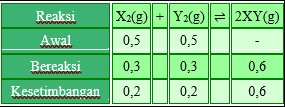
Kc = (0,6/V)2 : 0,2/V × 0,2/V
Kc = 0,36 : 0,4
Kc = 9
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 20 yaitu C
Soal OSK Kimia 2016 PDF Nomer 21
Dari reaksi kesetimbangan di bawah ini, manakah yang pada temperatur konstan bila tekanannya bertambah tidak merubah konsentrasi reaktan dan produk?
A. N2(g) + 3H2(g) ⇌ 2NH3(g)
B. 2N2(g) + O2(g) ⇌ 2N2O(g)
C. N2(g) + 2O2(g) ⇌ 2NO2(g)
D. N2O4(g) ⇌ 2NO2(g)
E. N2(g) + O2(g) ⇌ 2NO(g)
Pembahasan Soal OSK Kimia 2016 PDF Nomer 21
Pada temperatur tetap dan tekanan berubah konsentrasi reaktan dan produk tidak akan berubah bila jumlah zat-zat pereaksi dan produk setara. Jumlah zat ini (gas) sanggup dilihat pada jumlah koefisien ruas kiri dan ruas kanan sama. Di antara reaksi yang mempunyai jumlah koefisien ruas kiri dan kanan sama yaitu sama dengan 2 yaitu N2(g) + O2(g) ⇌ 2NO(g)
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 21 yaitu E
Soal OSK Kimia 2016 PDF Nomer 22
Dalam reaksi: CH2NH2 + H2PO4– → CH3NH3+ + HPO4–2
Ion H2PO4– adalah suatu:
A. Asam
B. Basa
C. Agen pengoksidasi
D. Agen pereduksi
E. Katalis
Pembahasan Soal OSK Kimia 2016 PDF Nomer 22
Reaksi CH2NH2 + H2PO4– → CH3NH3+ + HPO4–2 adalah reaksi asam basa Bronsted-Lowry,
atau reaksi transfer proton (H+)
Zat yang memberi H+ disebut sebagai asam.
Zat yang mendapatkan H+ disebut sebagai basa.
Tampak bahwa ion H2PO4– → HPO4–2 + H+ (selanjutnya H+ ini diterima CH2NH2 yang berepran sebagai basa).
Jadi ion H2PO4– ini berperan sebagai asam.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 22 yaitu A
Soal OSK Kimia 2016 PDF Nomer 23
Pada 0oC, konstanta produk ion dari air, Kw = 1,2 × 10–15. Nilai keasaman (pH) dari air murni pada 0oC yaitu :
A. 7,00
B. 6,88
C. 7,56
D. 7,46
E. 7,64
Pembahasan Soal OSK Kimia 2016 PDF Nomer 23
[H+ ]=[OH–]
Kw = [H+ ][OH–]
Kw = [H+ ]2
[H+] = √(1,2 ×10–15) → 3,4641 ×10–8
pH = -log (3,4641 ×10–8) → pH = 7,46
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 23 yaitu D
Soal OSK Kimia 2016 PDF Nomer 24
Bila 100 mL larutan 0,100 M KOH dicampurkan dengan 100 mL larutan yang mengandung HCl 0,075 M dan asam asetat (CH3COOH) 0,050 M maka larutan yang terbentuk mengandung spesi-spesi:
A. K+, Cl–, CH3COO–, CH3COOH
B. Cl–, CH3COO–, CH3COOH, dan H+
C. CH3COOH, CH3COO–, OH– dan H+
D. K+, Cl–, CH3COOH dan H+
E. K+, Cl–, CH3COO–, CH3COOH, OH– dan H+
Pembahasan Soal OSK Kimia 2016 PDF Nomer 24
KOH dalam air terurai menjadi K+ dan OH–, HCl dalam air terurai menjadi H+ dan Cl–, CH3COOH dalam air tidak sanggup terurai total sehingga akan terdapat CH3COOH yang tersisa serta CH3COO–dan H+. Kaprikornus secara keseluruhan dalam adonan larutan tersebut terdapat K+, Cl–, CH3COO–, CH3COOH, OH– dan H+
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 24 yaitu E
Soal OSK Kimia 2016 PDF Nomer 25
Sebanyak 100 mL larutan NaOH yang mempunyai pH =12, ditambahkan sebanyak 900 mL air. Nilai pH larutan yang anda peroleh adalah:
A. 1
B. 3
C. 7
D. 11
E. 13
Pembahasan Soal OSK Kimia 2016 PDF Nomer 25
pH NaOH = 12 → pOH = 14 – 12 = 2 → [OH–] = 0,01 M
V1.M1 = V2.M2
100 × 0.01 = (100+900) × M2
M2 = 1/1000 = 0,001 M
[OH–] = 0,001 → pOH = -log 0,001 = 3
pH = 14 – 3 = 11
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 25 yaitu D
Soal OSK Kimia 2016 PDF Nomer 26
Bila anda menciptakan larutan asam lemah ibarat tabel di bawah ini dengan molaritas yang sama, maka yang akan memperlihatkan pH paling kecil adalah: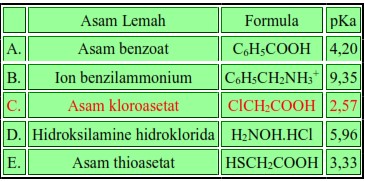
Pembahasan Soal OSK Kimia 2016 PDF Nomer 26
Asam lemah dengan konsentrasi masing-masing 1 M
→ pH = –log(√(Ka.M))
→ pH = –½ log Ka – ½ log M
→ pH = ½ pKa – ½ log M
→ pH = ½ pKa – ½ log 1
→ pH = ½ pKa – 0
→ pH = ½ pKa
pH paling kecil diperoleh dari pKa paling kecil.
pH paling kecil = ½ 2,57 = 1,285
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 26 yaitu C
Soal OSK Kimia 2016 PDF Nomer 27
Apa nama dari senyawa alkena berikut sesuai dengan hukum IUPAC?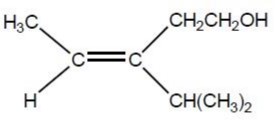
A. trans-3-isopropil-3-pentenol
B. cis-3-isopropil-3-pentenol
C. trans-3-dimetiletana-3-pentenol
D. (Z)-3-isopropil-3-penten-1-ol
E. (E)-3-isopropil-3-pentena-1-ol
Pembahasan Soal OSK Kimia 2016 PDF Nomer 27
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 27 yaitu E
Soal OSK Kimia 2016 PDF Nomer 28
Reaksi berikut ini: CH3CHO + H2O → CH3CH(OH)2 adalah reaksi:
A. Substitusi
B. Eliminasi
C. Esterifikasi
D. Kondensasi
E. Adisi
Pembahasan Soal OSK Kimia 2016 PDF Nomer 28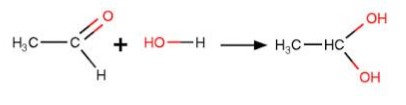
Ini yaitu reaksi adisi etanal (asetaldehid) oleh air menghasilkan etana-1,1-diol, ikatan rangkap pada gugus karbonil menjelma ikatan tunggal membentuk 2 gugus OH.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 28 yaitu E
Soal OSK Kimia 2016 PDF Nomer 29
Dalam kimia organik, kestabilan suatu senyawa sangat ditentukan oleh adanya substituen. Dari keempat isomer berikut, urutan kestabilan, dari yang paling tidak stabil hingga yang paling stabil, adalah:
A. I > III , IV > II
B. III , II > IV > I
C. IV > II, III > I
D. IV > I > II , III
E. III, IV > I > II
Pembahasan Soal OSK Kimia 2016 PDF Nomer 29
Semakin menyebar posisi substituen dalam suatu molekul organik maka akan dihasilkan tolakan antar substituen sekecil mungkin, dan ini akan membuatnya semakin stabil. Berdasarkan pilihan yang tersedia urutan kestabilannya yaitu IV > II, III > I
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 29 yaitu C
Soal OSK Kimia 2016 PDF Nomer 30
Senyawa alkohol kalau dipanaskan dalam suasana asam akan mengalami reaksi kekurangan cairan tubuh menghasilkan akena dengan kerangka yang berbeda dari kerangka senyawa semula, produk utama dari alkena yaitu yang sesuai dengan hukum Saytzeff. Manakah produk utama dari alkena yang terjadi di bawah ini?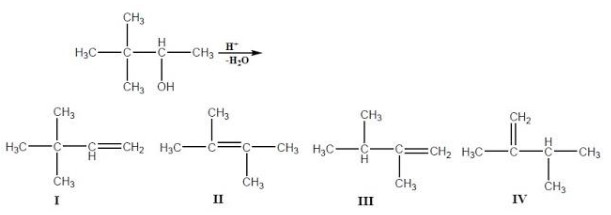
A. Hanya I
B. I dan IV
C. II dan III
D. I dan III
E. Hanya II
Pembahasan Soal OSK Kimia 2016 PDF Nomer 30
Pada pembentuk alkena dari alkohol berlaku hukum Saytzeff yaitu alkena yang lebih tersubstitusi akan menjadi produk utama. Alkena yang lebih tersubstitusi yaitu karbon sp2 (pada ikatan rangkap) yang mengikat substituen alkil lebih banyak. Tahapan reaksi menuju produk utama yaitu kekurangan cairan tubuh lalu dilanjut dengan penataan ulang gugus -CH3dan pelepasan H yang ditarik oleh HSO4–hingga menghasilkan produk utama 2,3-dimetil-2-butena.
Jadi, kunci tanggapan Soal OSK Kimia 2016 PDF Nomer 30 yaitu E
Demikian tadi soal, pembahasan dan kunci tanggapan soal pilihan ganda (pilgan) OSK atau Olimpiade Sains Nasional tingkat Kabupaten / Kota tahun 2016. Semoga dengan adanya pembahasan soal ini, murid-murid sanggup mempersiapkan seleksi OSK sebaik-baiknya.
Sebelum meninggalkan website, baca juga :
Pembahasan Soal OSK Kimia 2017 PDF
Pembahasan Soal OSK Kimia 2018 PDF
Pembahasan Soal OSN Kimia 2016 Tingkat Kabupaten (OSK) PDF
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon