Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 31 – 40 – Pembahasan Soal UN 2018 mata pelajaran kimia ini bertujuan untuk memudahkan murid mempersiapkan UN 2019, serta menambah wawasan bapak ibu guru untuk membekali murid-murid di sekolah. Selain pembahasan soal, disertai pula kunci balasan dan link d0wnl0ad soal UN 2018 mapel kimia. Soal UN Fisika, Biologi, Matematika, Geografi, Ekonomi, Sosiologi dan Bahasa akan saya update di lain waktu.
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 31 – 40
Soal UN Kimia 2018 nomer 31
Bahan pemutih pakaian biasa digunakan untuk menghilangkan noda pada serat kain. Cairan pemutih mengandung materi aktif senyawa natrium hipoklorit (NaClO). Untuk menghitung kadar NaClO dalam pemutih sanggup digunakan metode titrasi iodometri. Reaksi yang terjadi adalah:
- NaClO (l) + 2KI(aq) + 2HCl(aq) → NaCl(aq) + 2KCl(aq) + I2(l) + 2H2O(l)
- I2(l) + 2Na2S2O3 (aq) → 2NaI (aq) + Na2S4O6(aq)
Berdasarkan wacana tersebut, sifat kimia dari senyawa yang terdapat dalam pemutih yaitu ….
- koloid pelindung
- oksidator
- reduktor
- katalisator
- inhibitor
Pembahasan Soal UNBK Kimia 2018 nomer 31
Kunci Jawaban Soal UN Kimia 2018 nomer 31 : B
Zat Pemutih (NaClO) pada reaksi pertama mengalami reaksi reduksi. Tepatnya bilangan oksidasi Cl pada NaClO berubah dari +1 menjadi –1 pada Cl– (dalam NaCl atau KCl). Karena beliau mengalami reaksi reduksi maka beliau berperan sebagai oksidator.
Soal UN Kimia 2018 nomer 32
Perhatikan warta berikut!
Larutan I : sebanyak 30 gram urea CO(NH2)2 dilarutkan dalam 250 mL air, dan larutan membeku pada suhu -3,6oC
Larutan II : sebanyak 30 gram garam NaCl dilarutkan dalam 250 mL air, dan larutan membeku pada suhu 7,4oC
Berdasarkan data kedua larutan tersebut, harga tetapan penurunan titik beku molal pelarut yaitu …
(Mr CO(NH2)2 = 60; NaCl = 58,5).
- 1,80oC molal-1
- 3,60oC molal-1
- 5,07oC molal-1
- 37,7oC molal-1
- 20,2oC molal-1
Pembahasan Soal UNBK Kimia 2018 nomer 32
Kunci Jawaban Soal UN Kimia 2018 nomer 32 : A
Urea merupakan larutan nonelektrolit.
molalitas urea = (30 g : 60 g/mol) : 0,25 kg = 2 molal
∆Tb = molalitas urea × Kf
3,6 oC = 2 molal × Kf
Kf = 3,6 oC : 2 molal = 1,8 oC/molal
NaCl merupakan larutan elektrolit dengan i = 2.
molalitas NaCl = (30 g : 58,5 g/mol) : 0,25 kg = 2,05 molal
∆Tb = molalitas NaCl × Kf × i
7,4 oC = 2,05 molal × Kf × 2
Kf = 7,4 oC : 4,1 molal = 1,8 oC/molal
Soal UN Kimia 2018 nomer 33
Diketahui konfigurasi elektron unsur A dan B ada sebagai berikut:
A: 1s2 2s2 2p1
B: 1s2 2s2 2p6 3s2 3p5
Jika kedua unsur A dan B membentuk suatu senyawa, rumus kimia dan bentuk molekul yang benar yaitu ….

Pembahasan Soal UNBK Kimia 2018 nomer 33
Kunci Jawaban Soal UN Kimia 2018 nomer 33 : A
A: elektron valensinya 3
B: elektron valensinya 7, perlu 1 elektron untuk stabil sesuai hukum oktet.
A3 + B1 → AB3→ semua elektron A terpakai untuk berikatan, tanpa elektron bebas.
Dengan demikian rumus bentuk umum AX3 bentuk molekulnya segitiga datar.
Soal UN Kimia 2018 nomer 34
Cermati wacana berikut.
Agar tampak lebih indah dan bernilai jual tinggi, sendok besi dilapisi dengan logam perak melalui proses penyepuhan. Proses penyepuhan sendok besi dengan logam perak sanggup memakai sel elektrolisis menyerupai gambar berikut ini.
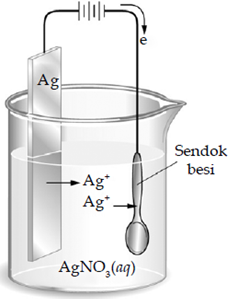
Pada proses penyepuhan sendok besi dengan logam perak (Ar = 108) pada wacana tersebut dilakukan selama 15 detik dengan memakai arus sebesar 9,65 ampere. Massa logam perak yang melapisi sendok adalah….
- 0,054 g
- 0,081 g
- 0,162 g
- 0,810 g
- 1,620 g
Pembahasan Soal UNBK Kimia 2018 nomer 34
Kunci Jawaban Soal UN Kimia 2018 nomer 34 : C
Ag+ + e– → Ag
Massa ekivalen Ag = 108; t = 15 detik; i = 9,65 ampere.
massa Ag yang digunakan untuk melapisi sendok
m = (e.i.t)/96.500
m = (108 × 9,65 × 15)/96.500
m = 0,162 gram
Soal UN Kimia 2018 nomer 35
Diketahui dua buah unsur X dan Y. Jika unsur X dan Y bersenyawa, sifat daya hantar listrik kalau senyawa tersebut dilarutkan dalam air dan jenis ikatan yang terjadi yaitu ….
- nonelektrolit dan kovalen koordinasi
- elektrolit dan ikatan kovalen koordinasi
- nonelektrolit dan ikatan kovalen
- elektrolit dan ikatan kovalen
- elektrolit dan ikatan ionik
Pembahasan Soal UNBK Kimia 2018 nomer 35
Kunci Jawaban Soal UN Kimia 2018 nomer 35
Soal tidak jelas
Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 31 – 40
Soal UN Kimia 2018 nomer 36
Perhatikan gambar berikut!
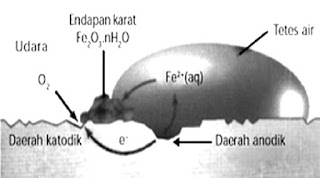 adanya oksigen dan uap air yang lembab menjadi penyebab terjadinya korosi
adanya oksigen dan uap air yang lembab menjadi penyebab terjadinya korosiKorosi atau proses perkaratan pada pipa bawah tanah merupakan proses elektronika kimia dengan reaksi:
Fe(s) → Fe2+ (aq) + 2e–
O2(g) + 4H+(g) + 4e– → 2H2O(l)
Untuk mencegah reaksi katodik, pipa dihubungkan dengan logam lain yang lebih gampang teroksidasi.
Berdasarkan warta tersebut, tamat yang sanggup didapat ihwal faktor-faktor penyebab korosi yaitu ….
- potensial reduksi Fe lebih besar dibanding dengan oksigen
- letak logam besi dalam deret Volta lebih kiri dari H2O
- adanya elektrolit/zat terlarut bersifat asam
- adanya oksigen dan uap air dalam udara yang lembab
- proses korosi mempunyai E0 reaksi yang negatif
Pembahasan Soal UNBK Kimia 2018 nomer 36
Kunci Jawaban Soal UN Kimia 2018 nomer 36 : D
Adanya oksigen dan uap air yang lembab menjadi penyebab terjadinya korosi
Soal UN Kimia 2018 nomer 37
Alat kompres hirau taacuh biasanya digunakan untuk mengurangi rasa sakit akhir cedera. Untuk kompres hirau taacuh biasanya digunakan garam amonium nitrat NH4NO3. Garam tersebut dikemas dalam kemasan yang juga berisi air, dikala ditekan kemasannya, 30 gram garam NH4NO3 akan bereaksi dengan 100 mL air dan sanggup menurunkan suhu dari 20oC menjadi 0oC dan sanggup bertahan sampai 20 menit.
Berdasarkan wacana tersebut, reaksi tersebut bersifat….
- eksoterm, energi berpindah dari sistem ke lingkungan
- eksoterm, energi berpindah dari lingkungan ke sistem
- endoterm, energi berpindah dari sistem ke lingkungan
- endoterm, energi berpindah dari lingkungan ke sistem
- endoterm, perubahan entalpi sistem berkurang
Pembahasan Soal UNBK Kimia 2018 nomer 37
Kunci Jawaban Soal UN Kimia 2018 nomer 37 : B
Karena reaksinya menyebabkan suhu turun maka reaksinya bersifat endoterm, proses perpindahan energi dari lingkungan ke sistem, sistem menyerap panas dari lingkungan.
Soal UN Kimia 2018 nomer 38
Cermati Wacana Berikut.
Bahan pemutih pakaian biasa digunakan untuk menghilangkan noda pada serat kain. Cairan pemutih mengandung materi aktif senyawa natrium hipoklorit (NaClO).
Untuk menghitung kadar NaClO dalam pemutih sanggup digunakan metode titrasi iodometri. Reaksi yang terjadi adalah:
- NaClO (l) + 2KI(aq) + 2HCl(aq) → NaCl(aq) + 2KCl(aq) + I2(l) + 2H2O(l)
- I2(l) + 2Na2S2O3 (aq) → 2NaI (aq) + Na2S4O6(aq)
Berdasarkan wacana tersebut, kalau dalam suatu percobaan titrasi terhadap 20 mL pemutih memerlukan sebanyak 40 mL Na2S2O3 0,2 M, kadar NaClO (w/w) dalam pemutih tersebut yaitu …. ( Mr NaClO = 74,5 dan r NaClO = 1 g/mL) .
- 0,745%
- 1,090%
- 1,117%
- 1,490%
- 2,235%
Pembahasan Soal UNBK Kimia 2018 nomer 38
Kunci Jawaban Soal UN Kimia 2018 nomer 38 : A
Massa NaClO kotor:
Massa NaClO = Volume NaClO × massa jenis NaClO
Massa NaClO = 20 mL × 1 g/mL
Massa NaClO = 20 g
Hitungan dari titrasi:
Perbandingan koefisien antara NaClO dengan koefisien Na2S2O3 = 1 : 2.
Jumlah mol Na2S2O3 yang dibutuhkan = 40 mL × 0,1 M = 4 mmol
Jadi jumlah mol NaClO = ½ × 4 mmol = 2 mmol = 0,002 mol
Massa NaClO = jumlah mol NaClO × massa molar NaClO
Massa NaClO = 0,002 mol × 74,5 g/mol
Massa NaClO = 0,149 g
Kadar NaClO = (massa NaClO titrasi : massa NaClO kotor) × 100%
Kadar NaClO = (0,149 g : 20 g) × 100%
Kadar NaClO = 0,745%
Soal UN Kimia 2018 nomer 39
Andi melaksanakan percobaan titrasi asam-basa untuk memperkirakan larutan asam oksalat (H2C2O4) dengan memakai indikator phenolftalein. Andi meneteskan larutan NaOH 0,1 M ke dalam larutan H2C2O4 (Mr H2C2O4 = 90 g/mol).
Data yang diperoleh dari tiga kali percobaan pada titik ekuivalen yaitu sebagai berikut.
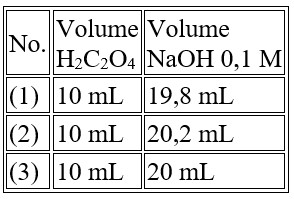
Jika massa jenis larutan asam oksalat 1,2 gram/mL, larutan asam oksalat tersebut mempunyai % massa H2C2O4 sebesar….
- 4,5%
- 3,5%
- 3,0%
- 1,5%
- 0,75%
Pembahasan Soal UNBK Kimia 2018 nomer 39
Kunci Jawaban Soal UN Kimia 2018 nomer 39 : E
Massa H2C2O4 = 10 mL × 1,2 g/mL = 12 g
Volume rata-rata NaOH = (19,8 + 20,2 + 20) mL : 3 = 20 mL
Jumlah mol NaOH = 20 mL × 0,1 M = 2 mmol.
Reaksi: 2NaOH + H2C2O4 → Na2C2O4 + 2H2O
Dari perbandingan koefisien reaksi setara dihitung jumlah mol H2C2O4 sebagai fakta.
Jumlah mol H2C2O4 = ½ jumlah mol NaOH
Jumlah mol H2C2O4 = ½ × 2 mmol
Jumlah mol H2C2O4 = 1 mmol = 0,001 mol
Massa H2C2O4dari hasil titrasi
Massa 0,001 mol H2C2O4 = 0,001 mol × 90 g/mol
Massa 0,001 mol H2C2O4 = 0,09 g
Kadar H2C2O4 = (massa H2C2O4 titrasi : massa H2C2O4 kotor) × 100%
Kadar H2C2O4 = (0,09 g : 12 g) × 100%
Kadar H2C2O4 = 0,75%
Soal UN Kimia 2018 nomer 40
Diketahui reaksi :

Jenis reaksi untuk nomor I, II, dan III berturut-turut yaitu ….
- adisi, substitusi, dan eliminasi
- adisi, substitusi, dan substitusi
- eliminasi, substitusi, dan adisi
- eliminasi, adisi, dan substitusi
- substitusi, adisi, dan adisi
Pembahasan Soal UNBK Kimia 2018 nomer 40
Kunci Jawaban Soal UN Kimia 2018 nomer 40 : B
I : jenis reaksi adisi, yang semula zat mempunyai ikatan rangkap menjadi ikatan tunggal.
II: jenis reaksi substitusi, ada atom H pada gugus CH2 di tengah propana digantikan 1 atom Br dari Br2
III: jenis reaksi substitusi, terjadi penggantian atom Br oleh gugus OH dari basa KOH.
=====
Sumber : urip.info
Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 1 – 10
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 11 – 20
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 21 – 30
Pembahasan Soal UNBK Kimia Tahun 2018 Nomer 31 – 40
Pembahasan Soal UNBK KIMIA Tahun 2018 Nomer 31 – 40
Sumber aciknadzirah.blogspot.com
EmoticonEmoticon